Формазаны
Формазаны (азогидразоны) — соединения общей формулы R1N=N-CR2=N-NHR3, формально являющиеся производными неизвестного в свободном виде формазана H2NN=CHN=NH (азогидразона муравьиной кислоты)[1]. Нумерация атомов и положение заместителей в формазанах отсчитываются от терминального атома азота азогруппы, наиболее изучены 1,5-ди- и 1,3,5-тризамещенные формазаны. Многие арил- и гетарилзамещенные формазаны ярко окрашены.
Реакционная способность
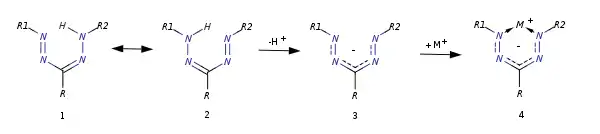
Связь N-H гидразонного азота легко диссоциирует и, вследствие этого для формазанов характерна таутомерия: 1,5-дизамещенные формазаны могут существовать в виде двух таутомеров 1 и 2. При депротонировании образующийся анион 3 стабилизирован за счет резонанса, с ионами переходных металлов (Cu2+, Co3+, Ni2+, Zn2+ и др.) формазаны образуют ярко окрашенные хелатные комплексы '4':
Формазаны являются амфотерными соединениями, способными протонироваться по терминальному атому азота азогруппы (так, рКа 1,5-дифенилформазана составляет ~ 16,5), 1,3,5-замещенные формазаны также алкилируются по терминальным атомам азота.
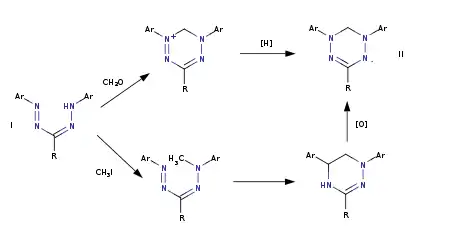
Такое алкилирование может происходить как под действием алкилгалогенидов или диалкилсульфатов, так и алифатических альдегидов по типу реакции Манниха. Образующиеся при конденсаци формазанов I с альдегидами вердазилиевые (дигидро-1,2,4,5-тетразиниевые) соли восстанавливаются до окрашенный в зеленый цвет свободных радикалов вердазилов II, устойчивых при нормальных условиях, такое восстановление может происходить при восстановлении вердазилиевых солей in situ избытком альдегида при проведении реакции в щелочной среде. Аналогичная циклизация протекает и при алкилировании формазанов, при этом первоначально образующиеся 5-алкилформазаны циклизуются в бесцветные лейковердазилы (тетрагидро-1,2,4,5-тетразины), которые окисляются кислородом воздуха в вердазилы:
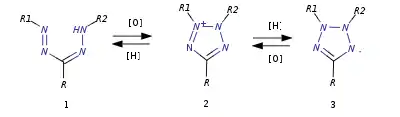
Формазаны под действием различных окислителей (хлор, N-бромсукцинимид, тетраацетат свинца и т. п.) циклизуются с образованием солей тетразолия, которые, в зависимости от условий, могут быть восстановлены до тетразолиевых свободных радикалов (действие амальгамы алюминия в присутствии пропиофенона), либо исходных формазанов:
Под действием восстановителей формазоны сначала происходит восстановление азогруппы с образованием гидразидинов, а затем, при действии энергичных восстановителях — разрыв связи N-N одного из гидразинных фрагментов с образованием амидразонов:
- R1C(=NNHR2)N=NR3 + [H] R1C(=NNHR2)NHNHR3
- R1C(=NNHR2)NHNHR3 + [H] R1C(=NNHR2)NH2
Углерод метиновой группы 1,5-диарилформазанов нуклеофилен: 1,5-формазаны галогенируются с образованием 3-галогенпроизводных, аминометилируются в условиях реакции Манниха и нитрозируются, образующиеся при этом 3-нитрозо-1,5-диарилформазаны изомеризуются в соответствующие арилазооксимы.
3-Галоген- и 3-нитроформазаны реагируют с нуклеофильными агентами, образуя соответствующие продукты замещения: так, реакция 1,5-дифенил-3-нитроформазана с тиомочевиной и образованием 1,5-дифенил-3-меркаптоформазана с его последующей перегруппировкой в тион является методом синтеза дитизона - реагента для фотометрического определения катионов переходных металлов.
Синтез
Формазаны могут быть синтезированы окислительным сочетанием альдегидов либо соответствующих им спиртов с замещенными гидразинами:
- RNHNH2 + CH3 OH + [O] HC(=NNHR)N=NR ,
в таком окислительном сочетании также могут быть использованы и гидразоны альдегидов.
Другим методом синтеза формазанов из гидразонов альдегидов и α-кетокислот является реакция азосочетания арилдиазониевых солей с такими гидразонами (в последнем случае диазосочетание сопровождается декарбоксилированием):
- Ar-N≡N+ + RCH=NNH2 RC(=NNH2)N=NAr
Вариацией этого метода является азосочетание арилдиазониевых солей с соединениями, содержащими активированную электронакцепторными заместителями метиленовую группу, при этом на начальном этапе диазотирования образуются соответствующие гидразоны, далее диазотирующиеся с потерей уходящей группы до формазанов:
- CH2(COOR)2 + Ar-N≡N+ ROOC-C(=NNAr)N=NAr
Формазаны также могут быть синтезированы из хлоргидразонов, получающихся при взаимодействии гидразидов с пятихлористым фосфором. На первой стадии арилгидразины ацилируются хлоргидразонами с образованием гидразидинов, которые далее окисляются до формазанов:
- RNHNH2 + R1C(Cl)=NNHR2 R1C(=NNHR2)NHNHR
- R1C(=NNHR2)NHNHR + [O] R1C(=NNHR2)N=NR
Применение

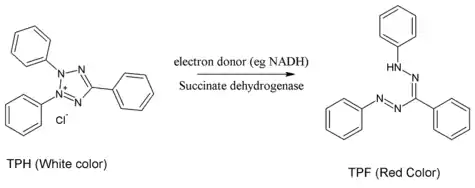
Образование окрашенных формазанов при ферментативном восстановлении тиазолиевых солей широко используется в гистохимии. В 1941 г. было показано, что тетразолиевые соли, не восстанавливающиеся при физиологических значениях pH присутствующими в клетках восстановителями (альдозы, глутатион, аскорбиновая кислота, цистеин), восстанавливаются живыми клетками[2] и в 1942 г. Г. Лаконом окраска ткани тетразолиевыми солями была предложена как метод определения жизнеспособности семян (топографический тетразольный метод) при окраске раствором хлоридом 2,3,5-трифенилтетразолия красная окраска, обусловленная образующимся формазаном, наблюдалась только на участках живой ткани, проявляющей ферментативную активность[3].
Варьирование заместителей тетразолиевого ядра используется для модификации свойств этих редокс-красителей, ниже приведены несколько часто используемых в биохимических исследованиях восстанавливающихся до окрашенных формазанов тетразолиевых солей[4]:
- INT — 2-(4-йодфенил)-3-(4-нитрофенил)-5-фенил-2H-тетразолия хлорид
- MTT — 3-(4, 5-диметил-2-тиазолил)-2, 5-дифенил-2H-тетразолия бромид
- XTT — 2,3-бис-(2-метокси-4-нитро-5-сульфофенил)-2H-тетразолий-5-карбоксанилид
- MTS — 3-(4,5-диметилтиазол-2-ил)-5-(3-карбоксиметоксифенил)-2-(4-сульфофенил)-2H-тетразолий
- TTC — 2,3,5-трифенил-2H-тетразолия хлорид
Хелатные соли формазанов с переходными металлами (обычно, медные и кобальтовые комплексы) используются в качестве красителей текстильных волокон.
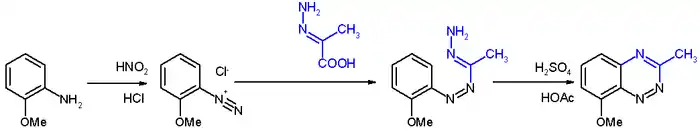
Циклизация арилформазанов в бенз-1,2,4-триазины под действием кислот является одним из первых методов синтеза 1,2,4-триазинов (синтез Бамбергера), сохранившим синтетическое значение и в настоящее время; сами исходные формазаны в классическом варианте метода синтезируются при взаимодействии диазониевых солей с гидразонами[5]:
Примечания
- formazans // IUPAC Gold Book
- Kuhn R, Jerchel D. Reduktion von Tetrazoliumsalzen durch Bakterien, garende Hefe und keimende Samen. Berichte der Deutshen Botanischen Gesellschaft 60:299–305. (1941)
- Lakon, G. Topographischer Nachweis der Keimfahigkeit der Getreidefruchte durch Tetrazoliumsalle. Ber. cler Dtsch. Bot. Ges. 60: 299·305. (1942)
- Altman F.P. Tetrazolium salts and formazans (неопр.) // Prog Histochem Cytochem. — 1976. — Т. 9, № 3. — С. 1—56. — PMID 792958.
- E.Bamberger, E.Wheelwright. Ber, 25, 3201 (1892