Молекулярная машина
Молекулярная машина, нанит или наномашина[1] – это молекулярный компонент, который производит квази-механические движения (выход) в ответ на определенные стимулы (вход)[2][3]. В клеточной биологии макромолекулярные машины часто выполняют жизненно важные задачи, такие как репликация ДНК и синтез АТФ. Выражение чаще всего применяется к молекулам, которые просто имитируют функции, происходящие на макроскопическом уровне. Этот термин также распространен в нанотехнологиях, где был предложен ряд очень сложных молекулярных машин, нацеленных на создание молекулярного ассемблера[4][5].
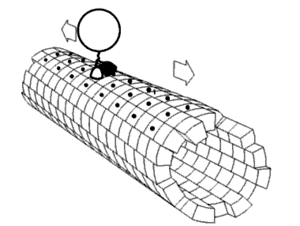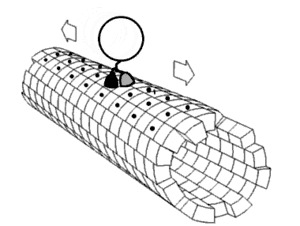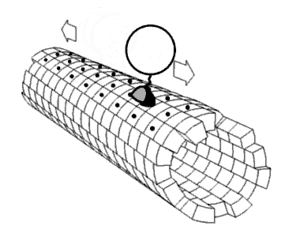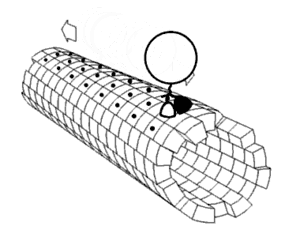
В течение последних нескольких десятилетий химики и физики с разной степенью успеха пытались миниатюризировать машины, существующие в макроскопическом мире. Молекулярные машины находятся в авангарде исследований клеточной биологии. Нобелевская премия по химии 2016 г. была присуждена Жан-Пьеру Соважу, сэру Дж. Фрейзеру Стоддарту и Бернарду Л. Феринге за разработку и синтез молекулярных машин[6][7].
Типы
Молекулярные машины можно разделить на две большие категории; искусственные и биологические. Искусственные молекулярные машины (АММ) относятся к молекулам, которые искусственно созданы и синтезированы, тогда как биологические молекулярные машины обычно встречаются в природе и эволюционировали в свои формы после абиогенеза на Земле[8].
Искусственные молекулярные машины
Химики синтезировали большое количество искусственных молекулярных машин (АММ), которые довольно просты и малы по сравнению с биологическими молекулярными машинами[8]. Первый молекулярный челнок AMM был синтезирован сэром Дж. Фрейзером Стоддартом[9]. Молекулярный челнок – это молекула ротаксана, в которой кольцо механически заблокировано на оси двумя громоздкими стопорами. Кольцо может перемещаться между двумя сайтами связывания с различными стимулами, такими как свет, pH, растворители и ионы[10].
Авторы статьи JACS 1991 года отмечали: «Поскольку становится возможным управлять движением одного молекулярного компонента по отношению к другому в ротаксане, появится технология для создания молекулярных машин». Механически взаимосвязанные молекулярные архитектуры возглавили разработку и синтез AMM, поскольку они обеспечивают направленное движение молекул[11]. Сегодня существует большое количество AMM, перечисленных ниже.
Молекулярные двигатели
Молекулярные двигатели – это молекулы, которые способны к направленному вращательному движению вокруг одинарной или двойной связи[12][13][14][15]. Роторные двигатели с одинарной связью[16] обычно активируются химическими реакциями, тогда как роторные двигатели с двойной связью[17] обычно работают от света. Скорость вращения двигателя также можно настроить с помощью тщательного молекулярного дизайна[18]. Также были произведены наномоторы из углеродных нанотрубок[19].
Молекулярный пропеллер
Молекулярный пропеллер – это молекула, которая может толкать жидкости при вращении благодаря своей особой форме, которая разработана по аналогии с макроскопическими пропеллерами[20][21]. У него есть несколько лезвий молекулярного масштаба, прикрепленных под определенным углом наклона по окружности наноразмерного вала. См. Также молекулярный гироскоп.
Молекулярный переключатель
Молекулярный переключатель – это молекула, которая может обратимо перемещаться между двумя или более стабильными состояниями[22]. Молекулы могут переключаться между состояниями в ответ на изменения pH, света (фотопереключатель), температуры, электрического тока, микросреды или присутствия лиганда[22][23][24].
Молекулярный челнок
Молекулярный челнок – это молекула, способная перемещать молекулы или ионы из одного места в другое[25]. Обычный молекулярный челнок состоит из ротаксана, макроцикл которого может перемещаться между двумя участками вдоль оси "гантели"[25][9][26].
Наномобиль (нанокар)
Нанокары – это одномолекулярные транспортные средства, которые напоминают макроскопические автомобили и важны для понимания того, как контролировать молекулярную диффузию на поверхностях. Первые наномобили были синтезированы Джеймсом М. Туром в 2005 году. У них было H-образное шасси и 4 молекулярных колеса (фуллерена), прикрепленных к четырем углам[27]. В 2011 году Бен Феринга и его сотрудники синтезировали первый моторизованный нанокар с молекулярными двигателями, прикрепленными к шасси в качестве вращающихся колес[28]. Авторам удалось продемонстрировать направленное движение наномобиля по поверхности меди, подавая энергию от острия сканирующего туннельного микроскопа. Позже, в 2017 году, в Тулузе прошла первая в мире гонка на нанокарах.
Молекулярные весы
Молекулярные весы[29][30] – это молекула, которая может взаимодействовать между двумя и более конформационными или конфигурационными состояниями в ответ на динамику множества внутри- и межмолекулярных движущих сил, таких как водородные связи, сольвофобные / гидрофобные эффекты[31], π-взаимодействия[32] стерические и дисперсионные взаимодействия[33]. Молекулярные весы могут состоять из небольших молекул или макромолекул, таких как белки. Кооперативно свернутые белки, например, использовались в качестве молекулярных весов для измерения энергии взаимодействия и конформационных склонностей[34].
Молекулярный пинцет
Молекулярный пинцет – это молекула-хозяин, способная удерживать предметы между двумя "руками"[35]. Открытая полость молекулярного пинцета связывает предметы с помощью нековалентных связей, включая водородные связи, координацию металлов, гидрофобные силы, силы Ван-дер-Ваальса, π-взаимодействия или электростатические эффекты[36]. Сообщалось о примерах молекулярных пинцетов, которые сконструированы из ДНК и считаются ДНК-машинами[37].
Молекулярный сенсор
Молекулярный сенсор – это молекула, которая взаимодействует с анализируемым веществом, вызывая обнаруживаемые изменения[38][39]. Молекулярные сенсоры сочетают молекулярное распознавание с некоторой формой репортера, поэтому присутствие объекта можно наблюдать.
Молекулярный логический шлюз
Молекулярный логический шлюз – это молекула, которая выполняет логическую операцию на одном или нескольких логических входах и производит единственный логический выход[40][41]. В отличие от молекулярного датчика, молекулярный логический шлюз будет выводить данные только при наличии определенной комбинации входов.
Молекулярный ассемблер
Молекулярный ассемблер – это молекулярная машина, способная управлять химическими реакциями, точно позиционируя реактивные молекулы[42][43][44][45][46].
Молекулярный шарнир
Молекулярный шарнир – это молекула, которую можно выборочно переключать с одной конфигурации на другую обратимым образом[47]. Такие конфигурации должны иметь различимую геометрию; например, азобензольные группы в линейной молекуле могут подвергаться цис- транс- изомеризации[48] при облучении ультрафиолетовым светом, вызывая обратимый переход к изогнутой или V-образной конформации[49][50][51][52]. Молекулярные шарниры обычно вращаются кривошипно вокруг жесткой оси, такой как двойная связь или ароматическое кольцо[53]. Однако также были синтезированы макроциклические молекулярные шарниры с механизмами, более похожими на зажим[54][55][56].
Биологические молекулярные машины
Самые сложные макромолекулярные механизмы находятся внутри клеток, часто в форме мультибелковых комплексов[57]. Важные примеры биологических машин включают моторные белки, такие как миозин, который отвечает за сокращение мышц, кинезин, который перемещает грузы внутри клеток от ядра по микротрубочкам, и динеин, который перемещает грузы внутри клеток к ядру и вызывает биение аксонемы подвижные реснички и жгутики. В результате подвижная ресничка представляет собой наномашину, состоящую из более чем 600 белков в молекулярных комплексах, многие из которых также функционируют независимо как наномашины. Гибкие линкеры позволяют соединенным ими мобильным белковым доменам привлекать своих партнеров по связыванию и вызывать дальнодействующую аллостерию через динамику белковых доменов[1]. За производство энергии отвечают другие биологические машины, например АТФ-синтаза, которая использует энергию протонных градиентов через мембраны, чтобы управлять турбиноподобным движением, используемым для синтеза АТФ, энергетической валюты клетки[58]. Другие машины отвечают за экспрессию генов, включая ДНК-полимеразы для репликации ДНК, РНК-полимеразы для производства мРНК, сплайсосомы для удаления интронов и рибосомы для синтеза белков. Эти машины и их наноразмерная динамика намного сложнее любых молекулярных машин, которые до сих пор были созданы искусственно[59].
Биологические машины могут найти применение в наномедицине. Например[60], их можно использовать для идентификации и уничтожения раковых клеток[61][62]. Молекулярная нанотехнология – это спекулятивное подразделение нанотехнологии, касающееся возможности разработки молекулярных ассемблеров, биологических машин, которые могут переупорядочивать материю в молекулярном или атомном масштабе. Наномедицина будет использовать этих нанороботов, введенных в организм, для восстановления или обнаружения повреждений и инфекций. Молекулярная нанотехнология в высшей степени теоретическая, она направлена на то, чтобы предвидеть, какие изобретения могут принести нанотехнологии, и предложить повестку дня для будущих исследований. Предлагаемые элементы молекулярной нанотехнологии, такие как молекулярные ассемблеры и нанороботы, намного превосходят существующие возможности[63][64].

Исследования
Создание более сложных молекулярных машин – активная область теоретических и экспериментальных исследований. Был разработан ряд молекул, таких как молекулярные пропеллеры, хотя экспериментальные исследования этих молекул затруднены из-за отсутствия методов их создания[65]. В этом контексте теоретическое моделирование может быть чрезвычайно полезным[66] для понимания процессов самосборки / разборки ротаксанов, важных для создания молекулярных машин с легким двигателем[67]. Эти знания на молекулярном уровне могут способствовать реализации все более сложных, универсальных и эффективных молекулярных машин для областей нанотехнологии, включая молекулярные ассемблеры.
Хотя в настоящее время это неосуществимо, некоторые потенциальные применения молекулярных машин включают транспортировку на молекулярном уровне, манипулирование наноструктурами и химическими системами, обработку твердотельной информации высокой плотности и молекулярное протезирование[68]. Прежде чем молекулярные машины можно будет использовать на практике, необходимо преодолеть многие фундаментальные проблемы, такие как автономная работа, сложность машин, стабильность в синтезе машин и рабочие условия[8].
Примечания
- Satir, Peter (2008-03-26). “Structure and function of mammalian cilia”. Histochemistry and Cell Biology. 129 (6): 687—93. DOI:10.1007/s00418-008-0416-9. PMID 18365235. 1432-119X.
- “Artificial Molecular-Level Machines: Which Energy To Make Them Work?”. Acc. Chem. Res. 34 (6): 445—455. 2001. DOI:10.1021/ar000170g. PMID 11412081.
- “The Future of Molecular Machines”. ACS Central Science. 6 (3): 347—358. March 2020. DOI:10.1021/acscentsci.0c00064. PMID 32232135.
- Drexler, K. E. (July 1991). “Molecular directions in nanotechnology”. Nanotechnology [англ.]. 2 (3): 113—118. Bibcode:1991Nanot...2..113D. DOI:10.1088/0957-4484/2/3/002. ISSN 0957-4484.
- Full Page Reload.
- Staff. The Nobel Prize in Chemistry 2016, Nobel Foundation (5 October 2016). Дата обращения 5 октября 2016.
- Chang. 3 Makers of 'World's Smallest Machines' Awarded Nobel Prize in Chemistry, New York Times (5 October 2016). Дата обращения 5 октября 2016.
- Erbas-Cakmak, Sundus (2015). “Artificial Molecular Machines”. Chemical Reviews. 115 (18): 10081—10206. DOI:10.1021/acs.chemrev.5b00146. PMID 26346838.
- Anelli, Pier Lucio (June 1991). “A molecular shuttle”. Journal of the American Chemical Society. 113 (13): 5131—5133. DOI:10.1021/ja00013a096. PMID 27715028.
- Bruns, Carson J. (30 May 2014). “Rotaxane-Based Molecular Muscles”. Accounts of Chemical Research. 47 (7): 2186—2199. DOI:10.1021/ar500138u. PMID 24877992.
- Kay, Euan R. (24 August 2015). “Rise of the Molecular Machines”. Angewandte Chemie International Edition. 54 (35): 10080—10088. DOI:10.1002/anie.201503375. PMID 26219251.
- Fletcher, Stephen P. (2005-10-07). “A Reversible, Unidirectional Molecular Rotary Motor Driven by Chemical Energy”. Science. 310 (5745): 80—82. Bibcode:2005Sci...310...80F. DOI:10.1126/science.1117090. ISSN 0036-8075. PMID 16210531.
- Perera, U. G. E. (January 2013). “Controlled clockwise and anticlockwise rotational switching of a molecular motor”. Nature Nanotechnology. 8 (1): 46—51. Bibcode:2013NatNa...8...46P. DOI:10.1038/nnano.2012.218. ISSN 1748-3395. PMID 23263725.
- Schliwa, Manfred (2003-04-17). “Molecular motors”. Nature. 422 (6933): 759—765. Bibcode:2003Natur.422..759S. DOI:10.1038/nature01601. PMID 12700770.
- van Delden, Richard A. (October 2005). “Unidirectional molecular motor on a gold surface” (PDF). Nature. 437 (7063): 1337—1340. Bibcode:2005Natur.437.1337V. DOI:10.1038/nature04127. ISSN 1476-4687. PMID 16251960.
- Kelly, T. Ross (9 September 1999). “Unidirectional rotary motion in a molecular system”. Nature. 401 (6749): 150—152. Bibcode:1999Natur.401..150K. DOI:10.1038/43639. PMID 10490021.
- Koumura, Nagatoshi (9 September 1999). “Light-driven monodirectional molecular rotor” (PDF). Nature. 401 (6749): 152—155. Bibcode:1999Natur.401..152K. DOI:10.1038/43646. PMID 10490022.
- Vicario, Javier (2005). “Controlling the speed of rotation in molecular motors. Dramatic acceleration of the rotary motion by structural modification”. Chemical Communications. 116 (47): 5910—2. DOI:10.1039/B507264F. PMID 16317472.
- Fennimore, A. M. (24 July 2003). “Rotational actuators based on carbon nanotubes”. Nature. 424 (6947): 408—410. Bibcode:2003Natur.424..408F. DOI:10.1038/nature01823. PMID 12879064.
- Simpson, Christopher D. (March 2004). “Nanosized Molecular Propellers by Cyclodehydrogenation of Polyphenylene Dendrimers”. Journal of the American Chemical Society. 126 (10): 3139—3147. DOI:10.1021/ja036732j. PMID 15012144.
- Wang, Boyang (2007). “Chemically Tunable Nanoscale Propellers of Liquids”. Physical Review Letters. 98 (26): 266102. Bibcode:2007PhRvL..98z6102W. DOI:10.1103/PhysRevLett.98.266102. PMID 17678108.
- Feringa, Ben L. (May 2000). “Chiroptical Molecular Switches” (PDF). Chemical Reviews. 100 (5): 1789—1816. DOI:10.1021/cr9900228. PMID 11777421.
- Knipe, Peter C. (2015). “Ion-mediated conformational switches”. Chemical Science. 6 (3): 1630—1639. DOI:10.1039/C4SC03525A. PMID 28694943.
- Kazem-Rostami, Masoud (2017). “Hünlich base derivatives as photo-responsive Λ-shaped hinges”. Organic Chemistry Frontiers. 4 (2): 224—228. DOI:10.1039/C6QO00653A.
- Bissell, Richard A (12 May 1994). “A chemically and electrochemically switchable molecular shuttle”. Nature. 369 (6476): 133—137. Bibcode:1994Natur.369..133B. DOI:10.1038/369133a0.
- Chatterjee, Manashi N. (2006-03-01). “Beyond Switches: Ratcheting a Particle Energetically Uphill with a Compartmentalized Molecular Machine”. Journal of the American Chemical Society. 128 (12): 4058—4073. DOI:10.1021/ja057664z. ISSN 0002-7863. PMID 16551115.
- Shirai, Yasuhiro (November 2005). “Directional Control in Thermally Driven Single-Molecule Nanocars”. Nano Letters. 5 (11): 2330—2334. Bibcode:2005NanoL...5.2330S. DOI:10.1021/nl051915k. PMID 16277478.
- Kudernac, Tibor (10 November 2011). “Electrically driven directional motion of a four-wheeled molecule on a metal surface”. Nature. 479 (7372): 208—211. Bibcode:2011Natur.479..208K. DOI:10.1038/nature10587. PMID 22071765.
- Paliwal, S. (1994-05-01). “Molecular Torsion Balance for Weak Molecular Recognition Forces. Effects of "Tilted-T" Edge-to-Face Aromatic Interactions on Conformational Selection and Solid-State Structure”. Journal of the American Chemical Society. 116 (10): 4497—4498. DOI:10.1021/ja00089a057. ISSN 0002-7863.
- Mati, Ioulia K. (2010-10-19). “Molecular balances for quantifying non-covalent interactions” (PDF). Chemical Society Reviews. 39 (11): 4195—205. DOI:10.1039/B822665M. ISSN 1460-4744. PMID 20844782.
- Yang, Lixu (2015-08-19). “Quantifying Solvophobic Effects in Nonpolar Cohesive Interactions”. Journal of the American Chemical Society. 137 (32): 10084—10087. DOI:10.1021/jacs.5b05736. ISSN 0002-7863. PMID 26159869.
- Li, Ping (2013-06-07). “Comprehensive Experimental Study of N-Heterocyclic π-Stacking Interactions of Neutral and Cationic Pyridines”. The Journal of Organic Chemistry. 78 (11): 5303—5313. DOI:10.1021/jo400370e. ISSN 0022-3263. PMID 23675885.
- Hwang, Jungwun (2016-07-04). “Distance-Dependent Attractive and Repulsive Interactions of Bulky Alkyl Groups”. Angewandte Chemie International Edition. 55 (28): 8086—8089. DOI:10.1002/anie.201602752. ISSN 1521-3773. PMID 27159670.
- Ardejani, Maziar S. (2017-08-15). “Using Cooperatively Folded Peptides To Measure Interaction Energies and Conformational Propensities”. Accounts of Chemical Research. 50 (8): 1875—1882. DOI:10.1021/acs.accounts.7b00195. ISSN 0001-4842. PMID 28723063.
- Chen, C. W. (July 1978). “Molecular tweezers: a simple model of bifunctional intercalation”. Journal of the American Chemical Society. 100 (15): 4921—4922. DOI:10.1021/ja00483a063.
- Klärner, Frank-Gerrit (December 2003). “Molecular Tweezers and Clips as Synthetic Receptors. Molecular Recognition and Dynamics in Receptor−Substrate Complexes”. Accounts of Chemical Research. 36 (12): 919—932. DOI:10.1021/ar0200448. PMID 14674783.
- Yurke, Bernard (10 August 2000). “A DNA-fuelled molecular machine made of DNA”. Nature. 406 (6796): 605—608. Bibcode:2000Natur.406..605Y. DOI:10.1038/35020524. PMID 10949296.
- “Nanorobot architecture for medical target identification”. Nanotechnology. 19 (1): 015103(15pp). 2008. Bibcode:2008Nanot..19a5103C. DOI:10.1088/0957-4484/19/01/015103.
- Wu, Di (2017). “Fluorescent chemosensors: the past, present and future”. Chemical Society Reviews. 46 (23): 7105—7123. DOI:10.1039/C7CS00240H. PMID 29019488.
- Prasanna de Silva, A. (April 2000). “Proof-of-Principle of Molecular-Scale Arithmetic”. Journal of the American Chemical Society. 122 (16): 3965—3966. DOI:10.1021/ja994080m.
- Magri, David C. (April 2006). “Communicating Chemical Congregation: A Molecular AND Logic Gate with Three Chemical Inputs as a "Lab-on-a-Molecule" Prototype”. Journal of the American Chemical Society. 128 (15): 4950—4951. DOI:10.1021/ja058295+. PMID 16608318.
- Lewandowski, Bartosz (2013-01-11). “Sequence-Specific Peptide Synthesis by an Artificial Small-Molecule Machine”. Science. 339 (6116): 189—193. Bibcode:2013Sci...339..189L. DOI:10.1126/science.1229753. ISSN 0036-8075. PMID 23307739.
- De Bo, Guillaume (2014-04-16). “Efficient Assembly of Threaded Molecular Machines for Sequence-Specific Synthesis”. Journal of the American Chemical Society. 136 (15): 5811—5814. DOI:10.1021/ja5022415. ISSN 0002-7863. PMID 24678971.
- De Bo, Guillaume (2017-08-09). “Sequence-Specific β-Peptide Synthesis by a Rotaxane-Based Molecular Machine” (PDF). Journal of the American Chemical Society. 139 (31): 10875—10879. DOI:10.1021/jacs.7b05850. ISSN 0002-7863. PMID 28723130.
- Kassem, Salma (September 2017). “Stereodivergent synthesis with a programmable molecular machine”. Nature. 549 (7672): 374—378. Bibcode:2017Natur.549..374K. DOI:10.1038/nature23677. ISSN 1476-4687. PMID 28933436.
- De Bo, Guillaume (2018-04-02). “An artificial molecular machine that builds an asymmetric catalyst”. Nature Nanotechnology. 13 (5): 381—385. Bibcode:2018NatNa..13..381D. DOI:10.1038/s41565-018-0105-3. ISSN 1748-3395. PMID 29610529.
- Kay, Euan R. (January 2007). “Synthetic Molecular Motors and Mechanical Machines”. Angewandte Chemie International Edition. 46 (1–2): 72—191. DOI:10.1002/anie.200504313.
- Bandara, H. M. Dhammika (2012). “Photoisomerization in different classes of azobenzene”. Chem. Soc. Rev. 41 (5): 1809—1825. DOI:10.1039/c1cs15179g.
- Wang, Jing (2020). “Reversible photo-responsive gel–sol transitions of robust organogels based on an azobenzene-containing main-chain liquid crystalline polymer”. RSC Advances. 10 (7): 3726—3733. DOI:10.1039/C9RA10161F.
- Hada, Masaki (13 September 2019). “Ultrafast isomerization-induced cooperative motions to higher molecular orientation in smectic liquid-crystalline azobenzene molecules”. Nature Communications [англ.]. 10 (1): 4159. DOI:10.1038/s41467-019-12116-6. ISSN 2041-1723.
- Garcia-Amorós, Jaume (2014). “A photoswitchable bis-azo derivative with a high temporal resolution”. Chem. Commun. 50 (78): 11462—11464. DOI:10.1039/C4CC05331A.
- Kazem-Rostami, Masoud (2017). “Design and synthesis of Ʌ-shaped photoswitchable compounds employing Tröger's base scaffold”. Synthesis. 49 (6): 1214—1222. DOI:10.1055/s-0036-1588913.
- Kassem, Salma (2017). “Artificial molecular motors”. Chemical Society Reviews. 46 (9): 2592—2621. DOI:10.1039/C7CS00245A.
- Jones, Christopher D. (7 May 2021). “High-Yielding Flow Synthesis of a Macrocyclic Molecular Hinge”. Journal of the American Chemical Society. DOI:10.1021/jacs.1c02891. ISSN 0002-7863.
- Despras, Guillaume (10 August 2017). “Photocontrol over Molecular Shape: Synthesis and Photochemical Evaluation of Glycoazobenzene Macrocycles”. Chemistry - A European Journal. 23 (45): 10838—10847. DOI:10.1002/chem.201701232.
- Nagamani, S. Anitha (November 2005). “Photoinduced Hinge-Like Molecular Motion: Studies on Xanthene-Based Cyclic Azobenzene Dimers”. The Journal of Organic Chemistry. 70 (23): 9304—9313. DOI:10.1021/jo0513616.
- Donald, Voet. Biochemistry. — 2011. — ISBN 9780470570951.
- Kinbara, Kazushi (2005-04-01). “Toward Intelligent Molecular Machines: Directed Motions of Biological and Artificial Molecules and Assemblies”. Chemical Reviews. 105 (4): 1377—1400. DOI:10.1021/cr030071r. ISSN 0009-2665. PMID 15826015.
- Protein Structure and Diseases. — Vol. 83. — P. 163–221. — ISBN 9780123812629. — doi:10.1016/B978-0-12-381262-9.00005-7.
- Amrute-Nayak, M. (2010). “Targeted Optimization of a Protein Nanomachine for Operation in Biohybrid Devices”. Angewandte Chemie. 122 (2): 322—326. DOI:10.1002/ange.200905200. PMID 19921669.
- Patel, G. M. (2006). “Nanorobot: A versatile tool in nanomedicine”. Journal of Drug Targeting. 14 (2): 63—7. DOI:10.1080/10611860600612862. PMID 16608733.
- Balasubramanian, S. (2011). “Micromachine-Enabled Capture and Isolation of Cancer Cells in Complex Media”. Angewandte Chemie International Edition. 50 (18): 4161—4164. DOI:10.1002/anie.201100115. PMID 21472835.
- Freitas, Robert A. Jr. (2005). “Current Status of Nanomedicine and Medical Nanorobotics” (PDF). Journal of Computational and Theoretical Nanoscience. 2 (4): 471. Bibcode:2005JCTN....2..471K. DOI:10.1166/jctn.2005.001.
- Nanofactory Collaboration
- Golestanian, Ramin (2005-06-10). “Propulsion of a Molecular Machine by Asymmetric Distribution of Reaction Products”. Physical Review Letters. 94 (22): 220801. arXiv:cond-mat/0701169. Bibcode:2005PhRvL..94v0801G. DOI:10.1103/PhysRevLett.94.220801. PMID 16090376.
- Drexler, K. Eric (1999-01-01). “Building molecular machine systems”. Trends in Biotechnology [англ.]. 17 (1): 5—7. DOI:10.1016/S0167-7799(98)01278-5. ISSN 0167-7799.
- Tabacchi, G. (2016). “Dethreading of a Photoactive Azobenzene-Containing Molecular Axle from a Crown Ether Ring: A Computational Investigation”. ChemPhysChem. 17 (12): 1913—1919. DOI:10.1002/cphc.201501160. PMID 26918775.
- Coskun, Ali (2011-12-05). “Great expectations: can artificial molecular machines deliver on their promise?”. Chem. Soc. Rev. 41 (1): 19—30. DOI:10.1039/c1cs15262a. ISSN 1460-4744. PMID 22116531.