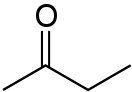
Метилэтилкетон
Метилэтилкето́н (систематическое наименование: бутано́н) — химическое соединение класса кетонов, второй член гомологического ряда алифатических кетонов. Химическая формула: .
| Метилэтилкетон | |||
|---|---|---|---|
| |||
 | |||
| Общие | |||
| Систематическое наименование |
Бутан-2-он | ||
| Хим. формула | |||
| Рац. формула | |||
| Физические свойства | |||
| Молярная масса | 72,12 г/моль | ||
| Плотность | 0,805 г/см³ | ||
| Энергия ионизации | 9,54 ± 0,01 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -86,3 °C | ||
| • кипения | 79,6 °C | ||
| • вспышки | 16 ± 1 ℉[1] | ||
| Пределы взрываемости | 1,4 ± 0,1 об.%[1] | ||
| Давление пара | 78 ± 1 мм рт.ст.[1] | ||
| Классификация | |||
| Рег. номер CAS | 78-93-3 | ||
| PubChem | 6569 | ||
| Рег. номер EINECS | 201-159-0 | ||
| SMILES | |||
| InChI | |||
| RTECS | EL6475000 | ||
| ChEBI | 28398 | ||
| ChemSpider | 6321 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
При обычных условиях — бесцветная, подвижная, легколетучая жидкость с запахом напоминающим запах ацетона. Обладает всеми химическими свойствами, характерными для алифатических кетонов.
Используется как растворитель и сырьё в органическом синтезе[2].
Получение
Промышленное производство
В промышленности метилэтилкетон получают из бутенов, содержащихся в бутан-бутиленовой фракции газов переработки нефти. На первой стадии производится гидратация бутенов 70—85%-ной серной кислотой () при 30—40 °C и давлении ~0,1 МПа в 2-бутанол с промежуточным образованием 2-бутилсульфата . 2-бутанол выделяют ректификацией и окисляют в метилэтилкетон дегидрированием при 400—500 °C (катализатор ZnO на пемзе или цинк-медный) или при 500 °C (в присутствии серебра на пемзе). Селективность гидратации бутенов составляет 80—85 %, дегидрирования 2-бутанола — около 99 %, окислительного дегидрирования — 85—90 %. Недостатки процесса: образование большого количества сточных вод на стадии гидратации, высокие энергозатраты, связанные с необходимостью концентрирования (в процессе гидратации разбавляется до 35%-ной концентрации).
Разработаны и внедрены (в Японии, ФРГ) процессы прямой гидратации бутенов с использованием гетерополикислот и сульфокатионитов в качестве катализаторов, не имеющие указанных недостатков. Перспективно получение метилэтилкетона окислением бутенов на гомогенном катализаторе — водном растворе соли палладия и обратимо действующего окислителя (например, фосфорномолибденванадиевой гетерополикислоты).
В лабораторных условиях метилэтилкетон можно получить дегидрированием 2-бутанола. Для идентификации метилэтилкетона синтезируют его производные: семикарбазон (температура плавления — 148 °C) или 2,4-динитрофенилгидразон (температура плавления — 115 °C).
Мировое производство метилэтилкетона ~800 тыс. т/год.
Физические свойства
С водой смешивается ограниченно, в любых пропорциях смешивается с большинством органических растворителей. Образует азеотропную смесь с водой (температура кипения 73,41 °С; 88,7 % по массе метилэтилкетона). Температура вспышки 2,2 °C, концентрационные пределы взрываемости — 1,97—10,2 %. В диапазоне этих концентраций взрывоопасен в смеси с воздухом.
Применение
Применяется как растворитель поливинилхлоридных, нитроцеллюлозных, полиакриловых лакокрасочных материалов и клеев, типографских красок, депарафинизации смазочных масел и обезмасливания парафинов (удаление смеси масла и низкоплавкого парафина); промежуточный продукт в производстве пероксида метилэтилкетона (отвердитель полиэфирных смол), втор-бутиламина и др.
Также применяется для производства чернил и разбавителя в каплеструйной технологии печати при использовании каплеструйных принтеров для маркировки продукции (сведения о дате производства, срока годности, партии и т. д.).
Является прекурсором некоторых наркотических веществ и в некоторых странах законодательство требует лицензии на использование, хранение и закупку.
Воздействие на человека
При концентрации 1 мг/л в течение 3—5 минут воздействия на человека вызывает раздражение слизистых оболочек глаз, носа и горла, 30 мг/л — раздражение становится невыносимым. ПДК рабочей зоны по ГОСТ 12.1.005-88 200 мг/м³.
Охрана труда
Легко воспламеняется, смесь с воздухом взрывоопасна при концентрации от 1,4 до 11,4 %[3]. Мгновенно-опасная концентрация 8850 мг/м³[4]
Метилэтилкетон — токсичное вещество[5]. По данным[6] ПДК в воздухе рабочей зоны равна 200 мг/м3 (среднесменная за 8 часов) и 400 мг/м3 (максимально-разовая). Порог восприятия запаха может достигать, например, 1000 мг/м3 [7] и 250 мг/м3[8]. Можно ожидать, что использование широко распространённых фильтрующих СИЗОД в сочетании с «заменой фильтров по появлении запаха под маской» (как это почти всегда рекомендуется в РФ поставщиками СИЗОД) приведёт к чрезмерному воздействию метилэтилкетона на, по крайней мере, часть работников — из-за запоздалой замены противогазных фильтров. Для защиты следует использовать значительно более эффективные изменение технологии и средства коллективной защиты.
Может попадать в организм и через кожу; поражаются глаза, центральная нервная система, кожа, органы дыхания[3].
Культура
Формула бутанона на пару как лекарство от болезни печени трижды упоминается в монологе Михаила Жванецкого «Тщательнее» (1987 год)[9].
Примечания
- http://www.cdc.gov/niosh/npg/npgd0069.html
- Чернышкова, 1992.
- Vern Anderson, Guss Hasbani, Heinz Ahlers, Barb Dames, Charles Geraci, Richard Niemeier, David Votaw, Alan Weinrich, and Ralph Zumwalde et al. 2-Butanone // NIOSH Pocket Guide to Chemical Hazards (англ.) / Michael E. Barsan (Technical Editor). — 3ed edition. — The National Institute for Occupational Safety and Health (NIOSH), 2007 (2010). — P. 36. — 454 p. — (DHHS (NIOSH) Publication No. 2005-149).
- NIOSH. Methyl ethyl ketone. Immediately Dangerous To Life or Health (IDLH) Values - Table of IDLH Values (англ.). www.cdc.gov/niosh/. The National Institute for Occupational Safety and Health (NIOSH) (2014). Дата обращения: 23 января 2020.
- МКХБ Международная организация труда. МКХБ № 0179. Метилэтилкетон. www.ilo.org/dyn/icsc/ (2018). Дата обращения: 12 ноября 2019.
- (Роспотребнадзор). № 411. Бутан-2-он (этилметилкетон) // ГН 2.2.5.3532-18 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны» / утверждены А. Ю. Поповой. — Москва, 2018. — С. 32. — 170 с. — (Санитарные правила).
- Artho. A. and R. Koch. Charactérisation Olfactive des Composés de la Fumee de Cigarettes (фр.) // Annales du tabac. Section 1. — Paris, 1973. — Vol. 2. — P. 37–43. — ISSN 0399-0206.
- Andrew Dravnieks. A building-block model for the characterization of odorant molecules and their odors (англ.) // The New York Academy of Sciences Annals of the New York Academy of Sciences. — New York: John Wiley & Sons, 1974. — September (vol. 237 (iss. 0). — P. 144—163. — ISSN 1749-6632. — doi:10.1111/j.1749-6632.1974.tb49851.x. — PMID 4529228.
- М. Жванецкий. Тщательнее.
Литература
- Юкельсон И. И. Технология основного органического синтеза. Стр. 354, 423, 445, 530, 539 сл., 581.
- Физер Л., Физер М. Органическая химия. Углубленный курс. (Том 1) Стр. 280, 461, 478.
- ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны.
- Чернышкова Ф. А. Метилэтилкетон // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Большая Российская энциклопедия, 1992. — Т. 3: Меди—Полимерные. — С. 68. — 639 с. — 48 000 экз. — ISBN 5-85270-039-8.