Изопроцессы
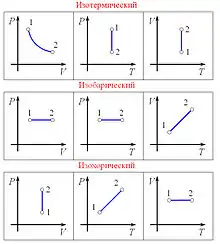
Изопроце́ссы — термодинамические процессы, во время которых количество вещества и один из параметров состояния: давление, объём, температура или энтропия — остаётся неизменным. Так, неизменному давлению соответствует изобарный процесс, объёму — изохорный, температуре — изотермический, энтропии — изоэнтропийный (например, обратимый адиабатический процесс). Линии, изображающие данные процессы на какой-либо термодинамической диаграмме, называются изобара, изохора, изотерма и адиабата соответственно. Изопроцессы являются частными случаями политропного процесса.
Изобарный процесс
Изоба́рный (или изобари́ческий) проце́сс (от др.-греч. ἴσος «равный» и βάρος «тяжесть, вес») — процесс изменения состояния термодинамической системы при постоянном давлении ().
Зависимость объёма газа от температуры при неизменном давлении была экспериментально исследована в 1802 году Жозефом Луи Гей-Люссаком. Закон Гей-Люссака: При постоянном давлении и неизменных значениях массы идеального газа и его молярной массы, отношение объёма газа к его абсолютной температуре остаётся постоянным: V/T = const.
Линия, изображающая изобарный процесс на диаграмме, называется изобарой.
Изохорный процесс
Изохо́рный (или изохори́ческий) проце́сс (от др.-греч. ἴσος «равный» и χώρος «[занимаемое] место») — процесс изменения состояния термодинамической системы при постоянном объёме (). Для идеальных газов изохорический процесс описывается законом Шарля: для данной массы газа при постоянном объёме, давление прямо пропорционально температуре:
Линия, изображающая изохорный процесс на диаграмме, называется изохорой.
Подведённая к газу теплота Q в изохорном процессе расходуется на изменение внутренней энергии U газа. Так, для одноатомного идеального газа
- Q = ΔU = 3⁄2νRT = 3⁄2V·ΔP,
где R — универсальная газовая постоянная,
- ν — количество молей газа,
- T — абсолютная температура в кельвинах,
- V — объём газа,
- ΔP — приращение давления.
Изотермический процесс
Изотерми́ческий проце́сс (от др.-греч. ἴσος «равный» и θέρμη «жар») — процесс изменения состояния термодинамической системы при постоянной температуре (). Изотермический процесс в идеальных газах описывается законом Бойля — Мариотта:
- При постоянной температуре и неизменных значениях массы газа и его молярной массы, произведение объёма газа на его давление остаётся постоянным: PV = const.
Изоэнтропийный процесс
Изоэнтропи́йный проце́сс — процесс изменения состояния термодинамической системы при постоянной энтропии (). Изоэнтропийным является, например, обратимый адиабатический процесс: в таком процессе не происходит теплообмена с окружающей средой. Идеальный газ в таком процессе описывается следующим уравнением:
где γ — показатель адиабаты, определяемый типом газа.