Эффект Караша
Эффект Караша (эффект Хараша, перекисный эффект) — обращение региоселективности при присоединении галогеноводородов к алкенам в присутствии кислорода или перекисей. Данный эффект, впервые описанный М. Карашем и Ф. Майо в 1933 году[1], заключается в образовании аномального продукта, формально не соответствующего правилу Марковникова. Это связывают с изменением механизма реакции, которая в данном случае протекает не как электрофильное присоединение, а как радикальное присоединение[2].

Механизм
Присоединение галогеноводородов к несимметричным алкенам в присутствии перекиси протекает по радикальному механизму. На стадии инициирования радикал R, полученный в результате разложения пероксидного катализатора, отщепляет от галогеноводорода атом водорода с образованием атома галогена, который на второй стадии присоединяется к двойной С=С-связи с образованием двух изомерных алкильных радикалов. Преобладающим является более замещённый, более устойчивый радикал, который затем реагирует с галогеноводородом, давая продукт — алкилгалогенид и атом галогена, продолжающий цепную радикальную реакцию[3].
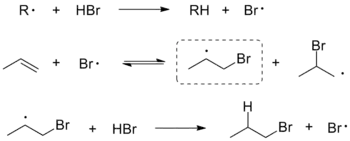
Реакция катализируется пероксидами, однако их добавление извне необязательно, поскольку в присутствии кислорода алкены могут сами окисляться с образованием перекисей[4]. Наряду с радикальной реакцией происходит также классическое электрофильное присоединение, однако радикальная реакция имеет гораздо более высокую скорость, за счёт чего аномальный продукт образуется в преобладающем количестве[4].
Считается, что данный эффект характерен исключительно для бромоводорода HBr и не наблюдается в случае других галогеноводородов (HF, HCl и HI)[3][5] за счёт того, что молекулы HF и HCl слишком прочны для гомолитического разрыва, а молекула HI хотя и имеет более низкую энергию связи, но образующийся атом йода недостаточно реакционноспособен и не может развить цепную реакцию. Тем не менее, известны примеры, когда HCl также реагирует с алкенами с образованием продуктов, не согласующихся с правилом Марковникова. Однако, такие примеры не очень распространены, и в общем случае при использовании HCl скорости электрофильного и радикального присоединения сопоставимы, что приводит к смеси продуктов[4]. Радикальное присоединение HCl к алкенам также может осложняться образованием олигомеров за счёт реакции алкильных радикалов с молекулами алкена[6].
Стереохимия присоединения
Реакции радикального присоединения галогеноводородов к алкенам протекают как анти-присоединение, что объясняется образованием циклического бромониевого радикала, раскрытие которого происходит «с тыла»[6]. При повышении температуры селективность снижается, поскольку становится возможным вращение С-С-связи в промежуточном алкильном радикале[4]. Для циклоалканов, в молекулах которых такое вращение невозможно, наблюдается образование только транс-продуктов[4].

См. также
Примечания
- Kharasch M. S., Mayo F. R. The Peroxide Effect in the Addition of Reagents to Unsaturated Compounds. I. The Addition of Hydrogen Bromide to Allyl Bromide (англ.) // J. Am. Chem. Soc. — 1933. — Vol. 55, no. 6. — P. 2468–2496. — doi:10.1021/ja01333a041.
- Робертс Дж., Касерио М. Основы органической химии = Basic Principles of Organic Chemistry / Пер. с англ. Ю. Г. Бунделя, под ред. А. Н. Несмеянова. — М.: Мир, 1978. — Т. 1. — С. 215—217.
- Терней А. Современная органическая химия. — М.: Мир, 1981. — Т. 1. — С. 323—324.
- Сайкс П. Механизмы реакций в органической химии = A Guidebook to Mechanism in Organic Chemistry / Под ред. Я. М. Варшавского. — 3-е изд.. — М.: Химия, 1977. — С. 290—293.
- Реутов О. А., Курц А. Л., Бутин К. П. Органическая химия. — 3-е изд.. — М.: Бином. Лаборатория знаний, 2010. — Т. 1. — С. 416. — ISBN 978-5-94774-613-6.
- Кери Ф., Сандберг Р. Углубленный курс органической химии / Под ред. В. М. Потапова. — М.: Химия, 1981. — Т. 1. — С. 476—478.