Циклопентадиен
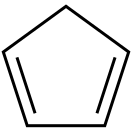
Циклопентадиен — циклический непредельный углеводород, жидкость с неприятным запахом.
| Циклопентадиен | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
1,3-циклопентадиен | ||
| Хим. формула | C5H6 | ||
| Физические свойства | |||
| Молярная масса | 66,1 г/моль | ||
| Плотность | 0,802 г/см³ | ||
| Энергия ионизации | 8,56 ± 0,01 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | −97 °C | ||
| • кипения | 41 °C | ||
| • вспышки | 0 °C | ||
| Давление пара | 435 мм. рт. ст. при 25 ℃ | ||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 0,00018 г/100 мл | ||
| Оптические свойства | |||
| Показатель преломления | 1,44 | ||
| Классификация | |||
| Рег. номер CAS | 542-92-7 | ||
| PubChem | 7612 | ||
| Рег. номер EINECS | 208-835-4 | ||
| SMILES | |||
| InChI | |||
| RTECS | GY1000000 | ||
| ChEBI | 30664 | ||
| ChemSpider | 7330 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Получение
Циклопентадиен получают из низкокипящих фракций продуктов пиролиза нефти и коксования каменного угля. Выделение циклопентадиена основано на его повышенной способности к димеризации, которая идёт уже при комнатной температуре. Смесь углеводородов димеризуется в реакторе при 100 ℃ в течение 5—14 часов, после чего дициклопентадиен отделяется ректификацией. Хранят и транспортируют циклопентадиен в виде димера[2].
В лабораторных условиях циклопентадиен может быть получен из 1,2-дибромциклопентана отщеплением HBr и дегидрированием циклопентена при 500—650 ℃ на алюмохромовом катализаторе.
Химические свойства
Циклопентадиен обладает свойствами диеновых углеводородов.
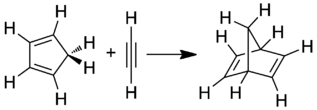
Вступает в реакции диенового синтеза. Например, с малеиновым ангидридом образует 5-норборнен-2,3-дикарбоновую кислоту, с ацетиленом — норборнадиен.
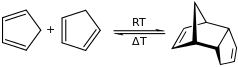
Легко димеризуется, димер разлагается при нагревании[2].
Обладает кислотными свойствами. Образует с металлами циклопентадиенильные π-комплексы[3].
Обесцвечивает бромную воду, так как является диеновым углеводородом.
Применение
Используется в органическом синтезе для получения инсектицидов альдрин и дильдрин (во многих странах запрещены к применению), ХЕТ-кислоты, используемой в производстве огнестойких красок[4], металлоценов, а также других соединений циклопентанового и норборненового ряда.
Примечания
- http://www.cdc.gov/niosh/npg/npgd0170.html
- Справочник нефтехимика. В двух томах / Под. ред. С. К. Огородникова. — Л.: Химия, 1978. — Т. 2. — С. 345. — 15 000 экз.
- Луис Физер, Мэри Физер. Органическая химия. Углубленный курс = Advanced organic chemistry / Под ред. Н. С. Вульфсона. — М.: Химия, 1966. — Т. 2. — С. 469. — 15 000 экз.
- Луис Физер, Мэри Физер. 5.38 Хлорированные аддукты // Органическая химия. Углубленный курс = Advanced organic chemistry / Под ред. Н. С. Вульфсона. — М.: Химия, 1966. — Т. 1. — 680 с. — 15 000 экз.