Триклопир
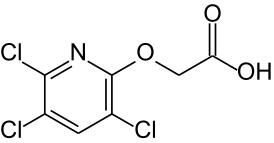
Триклопир — химическое соединение из группы пиридинкарбоновых кислот. Это пиридиновый аналог 2,4,5-трихлорфеноксиуксусной кислоты.
| Триклопир | |
|---|---|
   | |
| Общие | |
| Систематическое наименование |
[(3,5,6-трихлорпиридин-2-ил)окси]уксусная кислота |
| Хим. формула | C7H4Cl3NO3 |
| Физические свойства | |
| Молярная масса | 256,5 г/моль |
| Плотность | 1,85 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 150,5 °C |
| Химические свойства | |
| Константа диссоциации кислоты | 2,68 |
| Растворимость | |
| • в воде | 440 мг/л |
| • в ацетоне | 581 г/л |
| Классификация | |
| Рег. номер CAS | 55335-06-3 |
| PubChem | 41428 |
| Рег. номер EINECS | 259-597-3 |
| SMILES | |
| InChI | |
| ChEBI | 9682 |
| ChemSpider | 37801 |
| Безопасность | |
| ЛД50 | |
| Фразы риска (R) | R22 |
| Фразы безопасности (S) | S22 S24/25 |
| Краткие характер. опасности (H) |
H302 |
| Пиктограммы СГС |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Характеристики
Представляет собой белое твёрдое вещество, умеренно растворимое в воде[1]. Устойчив по отношению к гидролизу.
Синтез
Синтез триклопира начинается с пиридина, который хлорируется с образованием пентахлорпиридина. Атом хлора в пара-положении удаляется после реакции с гидразином. Получившейся 2,3,5,6-тетра-хлорпиридин реагирует с цианистым калием или цианистым натрием и триоксаном с образованием последнего промежуточного продукта, который карбоксилируется с соляной кислотой, превращаясь в триклопир[2].
Использование
Триклапир используется в качестве активного ингредиента гербицидов[1]. Он представляет собой системный селективный гербицид из класса аналогов растительных гормонов. Может применяться в качестве фунгицида[3].
Триклопир используется для контроля широколистных сорняков, в частности он эффективен против Бурды плющевидной, однако он безвреден для трав. Также он применяется для борьбы с ржавчинными заболеваниями культурных растений[3]. Он эффективен против деревьев и используется для дефолиации.
Триклопир производится как в виде сложных эфиров, так и в виде солей аммония. Химически он очень схож с гербицидом 2,4,5-T, которому часто служит заменой из-за сильной токсичности последнего.
Экология
В почве триклопир распадается с периодом полураспада от 30 до 90 дней. Один из продуктов его деградации, трихлорпиридинол, остаётся в почве вплоть до года. Триклопир быстро разлагается в воде. Он остается активным в гниющей растительности в течение 3-х месяцев.
Соединение слегка токсично для уток (ЛД50 = 1698 мг/кг) и перепелов (ЛД50 = 3000 мг/кг)[4]. Не токсично для пчёл и очень слабо токсично для рыб (Радужная форель LC50 (96 ч.) = 117 частей на миллион)[5].
Утверждение
Еврокомиссия включила триклопир в качестве гербицида в список разрешенных средств защиты растений 1 июня 2007 года[6].
В ряде государств ЕС, в частности в Германии и в Швейцарии триклопир разрешён к использованию, однако он запрещён в Австрии[7].
Примечания
- Record of CAS RN 55335-06-3 in the GESTIS Substance Database of the IFA.
- Thomas A. Unger. Pesticide Synthesis Handbook (неопр.). — William Andrew, 1996. — С. 540—541. — ISBN 0-81551853-6.
- Shanmugasundaram S.; Yeh C.C.; Hartman G.L.; Talekar N.S.;. Vegetable Soybean Research Needs for Production and Quality Improvement (англ.). — Taipei: Asian Vegetable Research and Development Center, 1991. — P. 86—87. — ISBN 9789290580478.
- EXTOXNET (Extension Toxicology Network), Oregon State University
- Environmental Fate Of Triclopyr Архивная копия от 13 июня 2009 на Wayback Machine, Carissa Ganapathy, Environmental Monitoring & Pest Management Branch Department of Pesticide Regulation Sacramento, CA
- Richtlinie 2006/74/EG der Kommission vom 21.
- Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Triclopyr in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz Архивная копия от 14 марта 2016 на Wayback Machine, Österreichs Архивная копия от 22 апреля 2016 на Wayback Machine und Deutschlands (недоступная ссылка) (недоступная ссылка) (недоступная ссылка) (недоступная ссылка) (недоступная ссылка); abgerufen am 20.