Стронгилоидоз
Стронгилоидо́з (лат. strongyloidosis, ангвиллюлёз, кохинхинская диарея) — паразитарное заболевание человека, вызываемое круглыми червями рода Strongyloides, преимущественно Strongyloides stercoralis. Характерной особенностью данных паразитов является способность с одной стороны жить и размножаться в организме хозяина десятилетиями практически бессимптомно, а с другой — вызывать угрожающие жизни состояния у людей со сниженным иммунитетом (диссеминированный стронгилоидоз со смертностью 60—85 %)[3].
| Стронгилоидоз | |
|---|---|
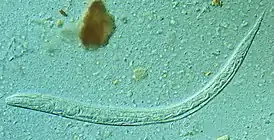 Личинка Strongyloides stercoralis | |
| МКБ-11 | 1F6B |
| МКБ-10 | B78 |
| МКБ-10-КМ | B78.9, B78, B78.7, B78.0 и B78.1 |
| МКБ-9 | 127.2 |
| МКБ-9-КМ | 127.2[1][2] |
| DiseasesDB | 12559 |
| MedlinePlus | 000630 |
| eMedicine | article/229312 |
| MeSH | D013322 |
Стронгилоидоз широко распространён в странах с тропическим и субтропическим климатом, и в эндемичных районах может поражать до 40 % населения. Всего по оценочным данным стронгилоидозом заражено от 100 до 200 млн человек в 70 странах мира[4].
Основной путь заражения стронгилоидозом — проникновение личинок червя через неповрежденную кожу при ходьбе босиком или при любом другом контакте с землёй. Симптомы могут отражать как процесс проникновения личинок, сопровождающийся зудом, так и пребывание червей внутри организма, где они разносятся током крови по сосудам и органам, в конечном итоге попадая в кишечник. Наиболее частые проявления инвазии — жидкий водянистый стул, боли в животе и уртикарная сыпь на коже.
Этиология
Причиной болезни являются круглые черви рода Strongyloides, из которых наиболее частый патоген — Strongyloides stercoralis (угрица кишечная). Из остальных 50 с лишним видов этого рода червей большинство безопасны для человека. Спорадически у больных из Африки и Папуа—Новой Гвинеи выделяется вид Strongyloides fuelleborni. Виды S. myopotami и S. procyonis имеют хозяевами животных и могут стать причиной зоонозных инфекций.
Распространённость
Стронгилоидоз распространён во влажных тропиках и субтропиках, в меньшей степени в зоне умеренного климата.Он относится к группе забытых тропических болезней[5], и всемирные усилия направлены на искоренение этой патологии. Встречается в Грузии (преимущественно в Абхазии и Аджарии), в Азербайджане, на западе Украины, в Российской Федерации: в Краснодарском, Ставропольском краях, Ростовской области, в Приамурье. В США болезнь распространена в южных штатах, на территориях заселенных приемущественно латино-американцами.
Механизм заражения
Свободноживущее поколение червей образует эндемичные очаги в почве. Половозрелые особи этого поколения откладывают яйца, из которых выходят рабдитиформные личинки. При неблагоприятных условиях окружающей среды они могут линять и, приобретая филяриевидную форму, внедряться через неповрежденную кожу человека. В месте внедрения личинок возникает местная воспалительная реакция.
Далее паразиты с током крови заносятся в лёгкие, откуда попадают в трахею и глотку, а затем заглатываются и попадают в кишечник. Здесь личинки созревают и превращаются во взрослых паразитических особей. Самец паразитического поколения погибает после копуляции, а самка начинает откладывать яйца, из которых прямо в кишечнике выходят рабдитиформные личинки. С испражнениями они попадают в почву и дают начало новому свободноживущему поколению червей.
Существует также механизм самозаражения (аутоинвазии), благодаря которому новые паразитические поколения образуются минуя свободноживущую фазу. Он заключается в том, что рабдитиформные личинки могут превращаться в инвазивные филяриевидные прямо в кишечнике при долгом нахождении в нём (например, при запорах). В этом случае перелинявшие личинки внедряются в стенку кишечника, по сосудам заносятся в лёгкие и цикл повторяется. Благодаря этому механизму стронгилоидоз может персистировать у человека десятилетиями, даже после выезда из очага.
Симптомы и признаки
Симптомы стронгилоидоза варьируют в широких пределах в зависимости от остроты болезни и индивидуальной реакции организма. Болезнь может протекать в нескольких формах: острая инфекция и синдром Лёффлера, хроническая инфекция с желудочно-кишечными проявлениями, асимптоматическая аутоинфекция, симптоматическая аутоинфекция и синдром гиперинфекции с диссеминацией (распространением) паразитов по всему организму [6].
У иммунокомпетентных лиц стронгилоидоз обычно принимает асимптоматическую или наиболее мягкую форму[7].
У ослабленных и иммунокомпрометированных лиц (имеющих раковые заболевания, СПИД, после трансплантации органов, химиотерапии и лечения кортикостероидами) стронгилоидоз может переходить в диссеминированную форму, когда личинки паразитов распространяются по всему организму[8]. Эта форма болезни может протекать тяжело, вызывая заражение крови (паразитемия), менингит, миокардит и др.
Желудочно-кишечные проявления
Симптомы могут быть очень разнообразными: боли в эпигастрии, вздутие живота, поносы и запоры, тошнота, рвота, снижение аппетита, потеря веса, анальный зуд. В классических случаях стул жидкий, водянистый, с примесью слизи, чередуется с запорами. Стронгилоидоз - важная причина отставания в развитии детей с пониженным иммунитетом.
Длительная инвазия может приводить к нарушению всасывания питательных веществ в кишечнике и синдрому мальабсорбции. Симптомы могут напоминать целиакию, включая стеаторею, гипоальбуминемию и периферические отёки.
Лёгочные проявления
Обусловлены миграцией личинок через альвеолы. Возникают примерно у 10% больных. Первичная инфекция может проявляться хрипами в лёгких и небольшим кашлем.
Миграция большого количества личинок приводит к пневмониту, напоминающему синдром Лёфлера. Симптомы включают продуктивный кашель, иногда с кровью, одышку и повышение температуры.
Стронгилоидоз может также проявляться симптомами, сходными с бронхиальной астмой и пневмонией.
Кожные проявления
Первичные кожные проявления обусловлены проникновением личинок. Чаще всего страдает кожа ног, но возможно появление высыпаний на любых участках, контактировавших с землёй. Сыпь представляет собой волдыри розово-красного цвета, овальной формы, возвышающиеся над поверхностью кожи. Они меняют форму, сопровождаются сильным зудом и «ползут» по коже со скоростью 5 - 15 см в час, в результате чего образуются линейной формы высыпания (larva currens). Сыпь держится от нескольких часов до нескольких дней, затем исчезает, но может появляться вновь, как аллергическая реакция при аутоинвазии новыми поколениями личинок.
Другие проявления
При поражении нервной системы могут наблюдаться головная боль, ригидность затылочных мышц, признаки менингита, в тяжелых случаях - коматозное состояние.
При распространении паразитов по всему организму (диссеминированная форма) может наблюдаться поражение печени, почек, сердца, брюшины, лимфатических узлов, поджелудочной и щитовидной железы, простаты, яичников. Сообщается о случаях аппендицита, вызванного инвазией S.stercoralis[9], а также эозинофильного оофорита[10].
Осложнения
Стронгилоидоз может давать осложнения на желудочно-кишечный тракт, лёгкие, сердце и другие органы, а также кожные и неврологические вплоть до летального исхода.
Желудочно-кишечные
- Нарушение усвоения питательных веществ (мальабсорбция)
- Кишечная непроходимость
- Аппендицит, перитонит
- Обструктивная желтуха
Лёгочные
- Бронхиальная астма или обострение существовавшей обструктивной болезни лёгких
- Пневмония
- Дыхательная недостаточность
- Острый респираторный дистресс-синдром
- Лёгочные кровотечения
- Плеврит
- Гранулёматоз лёгких
Прочие
Кожные осложнения включают «блуждающую личинку» (larva currens) — высыпания, появляющиеся в результате миграции под кожей личинок червя, пурпуру на теле и конечностях, а также хроническую крапивницу.
Неврологические осложнения могут включать менингит и абсцесс мозга, вызванные бактериями, попавшими из кишечника. К сосудистым осложнениям относится бактериемия (иногда повторная), вызванная также кишеными микроорганизмами (Escherichia coli, Klebsiella pneumoniae, Enterococcus sp., в том числе устойчивый к ванкомицину E. faecium, Streptococcus bovis).
Почечные осложнения иногда проявляются нефротическим синдромом. Исчезновение протеинурии при этом наблюдается после терапии антигельминтными препаратами (ивермектин). Нефротический синдром у детей в развивающихся странах чаще выявляется на фоне стронгилоидоза[11][12][13].
Диагностика
Диагностика стронгилоидоза может оказаться довольно трудной задачей, золотого стандарта для выявления болезни не существует. Зачастую диагноз выставляется очень поздно или неверно, из-за неспецифичности и размытости жалоб. У пациентов с хронической формой болезни количество живущих паразитов обычно невелико, личинки выделяются с калом нерегулярно и в малых количествах, что значительно затрудняет диагностику. Существует несколько основных методов диагностики:
- Микроскопия кала
- Модифицированный метод микроскопии по Берману[14]
- Культуральное исследование кала на кровяном агаре
- Иммуноферментный анализ (ИФА, ELISA)
- Реакция иммунофлуоресценции (IFAT)
- Полимеразная цепная реакция (ПЦР)
- Аспирационная биопсия
Лечение
Биохимические особенности паразита не позволяют достичь большого эффекта применением медикаментов в низких дозах. Личиночные стадии плохо поддаются терапии, лечение становится эффективнее при развитии болезни.
Препарат выбора для лечения стронгилоидоза — ивермектин. Он подходит для лечения острой и хронической формы, а также диссеминированной гиперинфекции. Процент выздоровления достигает 97 % после двухдневного курса. Препарат плохо изучен у детей.
Альтернативными препаратами являются альбендазол и мебендазол. Во избежание осложнений на ЦНС альбендазол может назначаться врачом в сочетании с антиконвульсантами и глюкокортикоидами.
Реабилитация больных достигается в течение 1 года. При длительном течении инвазии с развитием дистрофических изменений в слизистой оболочке желудочно-кишечного тракта может потребоваться приём ферментных препаратов и общеукрепляющих средств.
Прогноз
Прогноз при стронгилоидозе обычно благоприятный, если проводится соответствующая этиотропная терапия в наиболее ранние сроки. При возникновении осложнений (перфорация язвы при язвенном гастродуодените, кровотечение и др.), реинвазии и аутоинвазии, развитии интеркуррентных заболеваний на фоне сниженной реактивности организма (туберкулёз, воспалительные неспецифические заболевания и др.) прогноз может быть весьма серьёзным. Особенно тяжело протекает стронгилоидоз у больных СПИДом, так как сопровождается выраженными деструктивными изменениями в стенке кишки, иногда приводящими к перфорации, генерализации инвазии с поражением многих органов и систем, прежде всего ЦНС, лёгких и т. д.
Стронгилоидоз молодняка сельскохозяйственных животных
Заболевание телят, жеребят и поросят. Заражённые животные, более большей частью хронически, худеют, отстают в росте и плохо развиваются, а поросята в раннем возрасте часто гибнут. Заражение происходит в стойлах, хлевах и телятниках весной, летом и осенью. Свойство личинки проникать через неповрежденную кожу способствует массовому распространению[15].
Примечания
- база данных Disease ontology (англ.) — 2016.
- Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- Pranatharthi Haran Chandrasekar, MBBS, MD; Chief Editor: Burke A Cunha, MD. Strongyloidiasis (Updated: Jun 29, 2011). Дата обращения: 4 января 2013. Архивировано 6 января 2013 года.
- Genta RM. Global prevalence of strongyloidiasis: critical review with epidemiologic insights into the prevention of disseminated disease. // Rev Infect Dis.. — 1989; 11(5):755-67. — ISSN 0162-0886.
- Бронштейн А.М. и др. Острый и хронический стронгилоидоз у российских туристов, посетивших Таиланд, Черноморское побережье Краснодарского края и Абхазии: проблемы диагностики и лечения. анализ случаев и обзор литературы // Эпидемиология и инфекционные болезни. 2017; 22(3)
- Montes M, Sawhney C, Barros N. Strongyloides stercoralis: there but not seen // Curr Opin Infect Dis.. — Oct 2010;23(5):500-4.. — doi:10.1097/QCO.0b013e32833df718. — PMID PMC2948977.
- Montes M, Sanchez C, Verdonck K et al. Regulatory T cell expansion in HTLV-1 and strongyloidiasis co-infection is associated with reduced IL-5 responses to Strongyloides stercoralis antigen. // PLoS Negl Trop Dis.. — 2009 Jun 9;3(6):e456.. — doi:10.1371/journal.pntd.0000456..
- Roxby AC, Gottlieb GS, Limaye AP. Strongyloidiasis in transplant patients. // Clin Infect Dis.. — 2009 Nov 1;49(9):1411-23.. — doi:10.1086/630201.. — PMID 19807271.
- Komenaka IK, Wu GC, Lazar EL, Cohen JA. Strongyloides appendicitis: unusual etiology in two siblings with chronic abdominal pain. // J Pediatr Surg.. — Sep 2003;38(9):E8-10.. — ISSN 1531-5037.
- Butterfield JH, Kephart GM, Frankson JL. Eosinophilic oophoritis: association with positive Strongyloides stercoralis serology and clinical response to ivermectin. // J Pediatr Adolesc Gynecol.. — Oct 2006;19(5):329-32.. — ISSN 1083-3188.
- Morimoto J; Kaneoka H; Sasatomi Y et al. Disseminated strongyloidiasis in nephrotic syndrome. // Clin Nephrol.. — May 2002;57(5):398-401.. — ISSN 0301-0430.
- Hsieh YP, Wen YK, Chen ML. Minimal change nephrotic syndrome in association with strongyloidiasis. // Clin Nephrol.. — Dec 2006;66(6):459-63.. — ISSN 0301-0430.
- Copelovitch L, Sam Ol O, Taraquinio S, Chanpheaktra N. Childhood nephrotic syndrome in Cambodia: an association with gastrointestinal parasites. // J Pediatr.. — Jan 2010;156(1):76-81.. — ISSN 1097-6833.
- Берман Густав (Baermann Gustav Karl Theodor Friedrich ; 1877—1950) - немецкий врач, паразитолог, ученик Нейссера, работал на о. Ява, в 1917 году предложил свою методику извлечения личинок стронгилоидоза из кала и почвы.
- В.С.Ершов и др. Паразитология и инвазионные болезни сельскохозяйственных животных. — М., 1959. — 492 с.
Литература
- Шабловская Е. А. Стронгилоидоз. — М.: Медицина, 1986. — 128 с.
- Озерецковская Н. Н., Зальнова Н. С., Тумольская Н. И. Клиника и лечение гельминтозов. — Л.: Медицина. Ленингр. отд-ние, 1984. — 184 с. — (Библиотека практического врача. Инфекционные и паразитарные заболевания).
- Тропические болезни: Учебник / Е. П. Шувалова, Н. Н. Озерецковская, П. Н. Кашкин и др.; Под ред. Е. П. Шуваловой. — 3-е изд., перераб. и доп. — М.: Медицина, 1989. — 496, [16] с.
