Реакция Бухерера
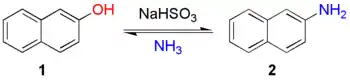
Реакция Бухерера (реакция Бухерера — Лепти) — реакция замещения гидроксильной группы на аминогруппу в ароматических соединениях (преимущественно в нафтолах) действием аммиака в водном растворе гидросульфита натрия. Реакция обратима: при нагревании нафтиламинов с водным раствором гидросульфитов происходит отщепление аммиака с образованием нафтолов:
Реакция впервые была описана в 1903 году Робертом Лепти и исследована в качестве синтетического метода Гансом Теодором Бухерером в 1904 году[1].
Механизм реакции
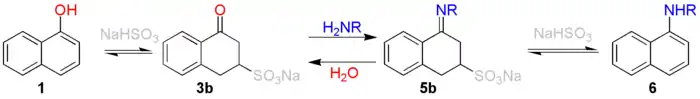
Реакция идет по механизму присоединения-отщепления. На первой стадии к фенолу (или к его еноновому таутомеру) присоединяется бисульфит-ион в β-положение к гидроксилу фенола 1 с образованием β-кетосульфокислоты 3b, в некоторых случаях эта сульфокислота может быть выделена. Эта стадия является лимитирующей, так, в случае β-нафтола и аммиака скорость реакции зависит только от концентраций нафтола и бисульфита. На следующей стадии к карбонильной группе β-кетосульфокислоты присоединяется аммиак (или первичный амин) с образованием имина 5b, которое затем таутомеризуется в енамин и отщепляет бисульфит-ион с образованием амина 6[2]:
Все стадии реакции Бухерера являются обратимыми, благодаря этому в условиях реакции возможно и трансаминирование первичных нафтиламинов действием алкиламинов во вторичные:
Синтетическое применение
В реакцию Бухерера вступают только ароматические гидрокси- и аминосоединения, способные к таутомеризации (кето-енольной и имин-аминной соответственно), в реакцию вступают нафтолы, замещенные гидрохиноны и резорцины и аза-аналоги нафтолов и нафтиламинов — гидрокси- и аминопроизводные хинолина и изохинолина, в последнем случае обмениваются гидрокси- и аминозаместители бензольного, но не пиридинового кольца.
Кроме аммиака, в качестве замещающего гидроксил агента в реакцию вступают и другие амины — так, при взаимодействии с нафтолами сульфита гидразина образуются нафтилгидразины, в жестких условиях нафтолы реагируют с первичными и вторичными алкиламинами с образованием N-моно- и N-диалкилнафтиламинов.
Наиболее широкое синтетическое применение реакция Бухерера получила в синтезе производных нафталина — полупродуктов синтеза азокрасителей, реакционная способность замещённых нафтолов зависит от типа и ориентации заместителей: реакционноспособными являются пара-замещённые нафтолы и нафтиламины (наиболее реакционноспособны 1-гидроксинафталин-4-сульфокислоты), в то время как нафтолы с карбоксильными и сульфогруппами в орто- и мета-положениях в реакцию не вступают. Это влияние заместителей позволяет проводить селективное замещение одной из гидрокси- или аминогруппы в дигидрокси- и диаминонафталинах.
Примечания
- H. Bucherer. Über die Einwirkung schwefligsaurer Salze auf aromatische Amido- und Hydroxylverbindungen (нем.) // Journal für Praktische Chemie : magazin. — 1904. — Bd. 69, Nr. 1. — S. 49—91. — doi:10.1002/prac.19040690105.
- Smith, Michael; Jerry March. March's Advanced Organic Chemistry: Reactions, Mechanisms, And Structure (англ.). — John Wiley & Sons, 2007. — P. 882—883. — ISBN 9780471720911.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1 (Абл-Дар). — 623 с.