Лейшмании
Лейшма́нии[5] (от имени У. Лейшмана) — род паразитических протистов, вызывающих лейшманиозы[6]. Переносчиками лейшманий являются москиты из рода Phlebotomus в Старом Свете, и из рода Lutzomyia в Новом Свете. Естественным резервуаром разных видов служат позвоночные животные, относящиеся к шести отрядам млекопитающих и ящерицам[7]; впрочем, на основании изоферментного анализа паразитов ящериц было предложено выделить в отдельный род отряда трипаносоматид — Sauroleishmania[8]. Лейшмании в основном поражают грызунов, собак и людей, но также отмечены случаи поражения у даманов, кошек и лошадей. В Новом Свете инфекция встречается у опоссумов, ленивцев и броненосцев[9]; зарегистрированы случаи лейшманиоза у кенгуру в Австралии[10]. По оценкам ВОЗ от начала 1990-х, лейшманиозами больны около 12 миллионов человек в 88 странах.
| Лейшмании | ||||||
|---|---|---|---|---|---|---|
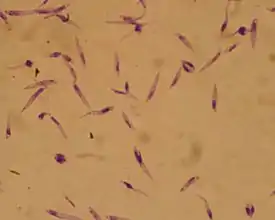 Промастиготы Leishmania major | ||||||
| Научная классификация | ||||||
|
Домен: Группа: Клада: Discoba Тип: Класс: Подкласс: Metakinetoplastina Отряд: Trypanosomatida Семейство: Род: Лейшмании |
||||||
| Международное научное название | ||||||
| Leishmania Ross, 1903 | ||||||
| Виды | ||||||
|
||||||
| ||||||
Происхождение
Происхождение лейшманий неясно[11][12]. Одна из теорий предполагает африканское происхождение, с последующей миграцией в Северную и Южную Америку. Другая — миграцию из Северной и Южной Америки через Берингов перешеек, около 15 миллионов лет назад. Третья предлагает палеарктическое происхождение[13].
Морфология
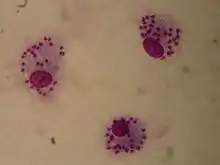
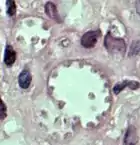
Лейшмании существуют в двух морфологических формах — промастиготы (с длинным передним жгутиком, веретенообразные, удлинённые, подвижные)[14] в насекомом-хозяине и на искусственных питательных средах, и амастиготы (с коротким жгутиком, круглые или овальные, неподвижные, расположенные внутриклеточно) в организме позвоночных.
Промастиготы разных видов практически неразличимы, но амастиготы некоторых видов возможно предположительно опознать по некоторым внешним признакам либо по характерному распределению внутри макрофагов. Так, амастиготы L. major обычно крупнее (4—5 микрон), чем L. tropica (1,5—2,5 микрон; оба эти вида сосуществуют в некоторых очагах), а число их внутри каждой клетки меньше: L. major, как правило, не больше десяти промастигот на макрофаг (обычно 2—4 амастиготы), в то время как L. tropica — до ста паразитов на клетку[15]. Leishmania mexicana часто располагается в крупных вакуолях по периферии клетки, формируя характерные «гирлянды»[16].
Жизненный цикл
Лейшмании, как и все трипаносоматиды, являются облигатными паразитами. Жизненный цикл лейшманий включает двух хозяев: млекопитающее и насекомое (москит).
Москиты заражаются лейшманиями, когда пьют кровь заражённого млекопитающего. Кровью питаются только самки москитов. Лейшмании вместе с проглатываемой кровью проникают в пищеварительный канал москита. В задней части средней кишки вокруг проглоченной крови у москита (как и у некоторых других кровососущих насекомых, например, комаров) образуется так называемая перитрофическая матрица.
Промастиготы лейшманий размножаются в пищеварительном тракте самок москитов. Приблизительно через неделю инфекция распространяется до верхних отделов пищеварительного тракта и паразиты блокируют просвет канала своими телами и секретируемым ими гелем. Когда самка кусает потенциального хозяина, она выделяет в кожу свою слюну. Самка с блокированным пищеварительным трактом не может глотать, и у неё возникают спастические движения, в результате которых она отрыгивает промастиготы в ранку на коже хозяина.
В среднем во время укуса инфицированным москитом в кожу попадает 100-1000 промастигот.
Первыми на место повреждения прибывают полиморфоядерные нейтрофилы, которые фагоцитируют паразитов. Внутри нейтрофилов лейшмании не размножаются и не превращаются в амастиготы. Затем, когда нейтрофилы переходят в фазу апоптоза, они уничтожаются макрофагами, и лейшмании проникают в макрофаги, не вызывая иммунного ответа[17]. Макрофаги являются основными клетками-хозяевами лейшманий в организме млекопитающих. Внутри макрофагов лейшмании трансформируются во внутриклеточную морфологическую форму — амастиготы.
Внутри макрофага лейшмании заключены в так называемые «паразитифорные вакуоли», которые образуются от слияния первичной фагосомы c лизосомами и эндосомами. В них промастиготы трансформируются в амастиготы. При этом происходят изменения в морфологии — продолговатые промастиготы с длинным жгутиком превращаются в овальные амастиготы с коротким жгутиком, в метаболизме, чтобы приспособиться к кислой среде, и в биохимическом составе мембраны. Трансформация занимает от двух до пяти дней. Амастиготы способны выживать в кислой среде этих вакуолей и питаться их содержимым. Внутри вакуоли амастиготы медленно размножаются, и каждый цикл размножения занимает около 24 часов.
При кожном лейшманиозе инфильтрат образуется в коже и содержит преимущественно макрофаги, а также лимфоидные клетки и немного плазматических клеток. При висцеральном лейшманиозе очаги инфекции образуются в органах ретикуло-эндотелиальной системы[18].
История открытия

Первое точное описание лейшмании в срезах кожных язв было опубликовано российским хирургом П. Ф. Боровским в «Военно-медицинском журнале» в 1898 году в статье «О сартовской язве». Боровский верно описал структуру паразитов и их отношение к тканям хозяина. Наблюдения Боровского подтвердил его коллега по Ташкентскому военному госпиталю Константин Яковлевич Шульгин в журнале «Русский врач» в 1902 г. В 1903 г. американский врач Райт опубликовал независимое описание паразитов в кожной язве у девочки из Армении, которое принципиально не отличалось от описания Боровского, но содержало качественные иллюстрации. Райт предложил для открытого организма название Helcosoma tropicum. По-видимому, Райт не знал о работе Боровского, а также о появившемся в том же году описании паразитов, вызывающих кала-азар, или не связал описание возбудителя кала-азара со своим[19].
В 1904 г. Марциновский и Богров опубликовали на русском и немецком описание возбудителя восточной язвы, снабжённое микрофотографиями, для которого они предложили название Ovoplasma orientale, причём, по всей видимости, работали они, не зная о работах Райта, хотя были знакомы с публикацией Боровского. В упомянутой статье они преуменьшают заслуги Боровского и неверно приводят его наблюдения. Хотя наблюдения Марциновского и Богрова опубликованы через несколько месяцев после Райта, их исследование было проведено на несколько месяцев раньше[19].
Классификация
В классификации лейшманий можно выделить четыре перекрывающихся периода. В начале XX в. основой классификации служили клинико-эпидемиологические и морфологические признаки, и лейшмании подразделялись на возбудителей висцерального лейшманиоза — L. donovani и возбудителей кожного лейшманиоза — L. tropica.
В 1913—1915 году В. Л. Якимов выделил два морфологических варианта возбудителя кожного лейшманиоза в Туркестане — с крупными или мелкими амастиготами — Leishmania tropica var. major и L. tropica var. minor[20], впоследствии они чаще обозначались как подвиды, без обозначения «var.». В 1940-х годах Кожевников и Латышев связали эти морфологические разновидности с двумя разными формами кожного лейшманиоза — антропонозным (L. tropica) и зоонозным (L. major)[21]. Впоследствии эти два подвида было предложено считать отдельными видами — L. tropica и L. major на основании клинико-эпидемиологических особенностей[22][23]. Морфологическая классификация применяется на практике и в начале XXI века; так, в провинции Балх на севере Афганистана, где встречается инфекция обоими этими видами, вид лейшманий определяют микроскопически на основании размера и количества амастигот в мазках из язв[15].
Тенденция считать возбудителей кожного лейшманиоза подвидами L. tropica просуществовала довольно долго. Так, в 1953 году Biagi предложил назвать описанного им возбудителя кожного лейшманиоза в Центральной Америке L. tropica var. mexicana[16].
Серологические методы классификации лейшманий начали применяться с середины 1910-х годов. Они позволяли отличать виды или комплексы видов. Реакция агглютинации и реакция связывания комплемента показали, что L. donovani и L. infantum серологически неразличимы. В 1930-х годах использование антисывороток позволило различить эти два вида[24]. В дальнейшем, с применением моноклональных антител, стало возможно различать отдельные серотипы внутри видов[25].
Характеризация лейшманий методом электрофореза изоферментов разрабатывалась с 1970-х годов начиная с отдельных ферментов[26], затем комбинаций ферментов[27][28]. Для обеспечения достаточной разрешающей способности требуется применять системы из многих ферментов — десяти до пятнадцати[29]. Штаммы организмов с одинаковыми электрофоретическими профилями называются «зимодем».
Наиболее полный банк лейшманий, охарактеризованных изоферментным анализом, хранится в университете Монпелье 1. Характеризация проводится на основании электрофореза 15 изоферментов с 1981 года. Начиная с 1989 года применяется метод изоэлектрического фокусирования[30], который имеет более высокую разрешающую способность, но применим только к шести ферментам[31].
Изоферментный анализ в последние четверть века является стандартным методом типирования лейшманий на видовом и подвидовом уровнях, потому что он был применён к наибольшему количеству самых разнообразных штаммов по сравнению с другими методами[32].
Зимодемы в лаборатории Монпелье получают обозначение, состоящее из сокращения MON (Монпелье), за которым следует порядковый номер зимодема. По состоянию на 2008 год, в лаборатории хранится более 3000 образцов лейшманий, разделённых на более чем 260 зимодемов.
Генетические методы, основанные на ПЦР, начали применяться с 1970-х годов. Эти методы имеют некоторые ограничения. В частности, изучение гетерозиготности и рекомбинации недостаточно разработаны для видов, в жизненном цикле которых нет гаплоидной стадии[32].
Разные методы классификации в основном совпадают в определении комплексов видов и генетических связей между ними.
На основании хода инфекции в моските-переносчике, род Leishmania делится на два подрода: Leishmania (Leishmania) и Leishmania (Viannia). Представители подрода Leishmania прикрепляются к эпителию средней кишки москита, а подрода Viannia — также к эпителию задней кишки. Представители подрода Leishmania распространены в Старом и Новом Свете, а подрода Viannia — только в Новом Свете[8].
Паразитов рептилий одни авторы выделяют в третий подрод лейшманий — Leishmania (Sauroleishmania), другие рассматривают его как отдельный род трипаносоматид — Sauroleishmania[8].
Геномика
Геномы трёх видов (L. major, L. infantum и L. braziliensis) были отсеквенированы, при этом было выявлено более 8300 генов белков и 900 генов РНК. Почти 40 % белок-кодирующих генов были распределены по 662 семействам, содержащим от 2 до 500 генов. Небольшие семейства в основном представлены генами, образующими тандемные повторы в различных локусах по всему геному. Каждая из 35 или 36 хромосом организована в небольшое число кластеров из 10—100 генов, расположенных на одной цепи ДНК. Эти кластеры могут быть расположены «голова к голове» (расходящиеся) или хвост к хвосту (сходящиеся). В последнем случае они могут быть разделены генами рРНК, тРНК или мяРНК. Транскрипция белок-кодирущих генов начинается в области расхождения кластеров и продолжается полицистронно до области переключения цепей между сходящимися кластерами.
Теломеры лейшманий обычно относительно короткие и состоят из нескольких типов повторяющихся последовательностей[33].
В 2009 году было показано, что в организме насекомого у лейшманий происходит процесс обмена генетической информацией, предполагающий мейоз[34].
Примечания
- Kuhls K. et al. Analysis of ribosomal DNA internal transcribed spacer sequences of the Leishmania donovani complex (англ.) // Microbes and Infection : journal. — 2005. — Vol. 7, no. 11—12. — P. 1224—1234. — PMID 16002315.
- Названо в честь Гашпара Вианна
- Lukeš J. et al. Evolutionary and geographical history of the Leishmania donovani complex with a revision of current taxonomy (англ.) // Proceedings of the National Academy of Sciences : journal. — National Academy of Sciences, 2007. — Vol. 104, no. 22. — P. 9375—9380. — doi:10.1073/pnas.0703678104.
- Schönian G. et al. Leishmaniases in the Mediterranean in the era of molecular epidemiology (англ.) // Trends in Parasitology : journal. — Cell Press, 2008. — Vol. 24, no. 3. — P. 135—142. — doi:10.1016/j.pt.2007.12.006. (недоступная ссылка)
- Лейшма́нии: Большая советская энциклопедия. 2-е изд. М., 1955. Т. 24. С. 360; в орфографических словарях также лейшмани́и :
- Ryan KJ; Ray CG (editors). Sherris Medical Microbiology (неопр.). — 4th ed.. — McGraw-Hill Education, 2004. — С. 749—754. — ISBN 0838585299.
- Noyes H.A. et al. The Leishmania hertigi (Kinetoplastida; Trypanosomatidae) complex and the lizard Leishmania: their classification and evidence for a neotropical origin of the Leishmania-Endotrypanum clade (англ.) // Journal of Eurkaryotic Microbiology : journal. — 1997. — Vol. 44, no. 5. — P. 511—517. — doi:10.1111/j.1550-7408.1997.tb05732.x.
- Rioux J.-A. et al. Taxonomy of Leishmania. Use of isoenzymes. Suggestions for a new classification (англ.) // Annales de parasitologie humaine et comparée : journal. — 1990. — Vol. 65, no. 3. — P. 111—125.
- Gramiccia M. and Gradoni L. The current status of zoonotic leishmaniases and approaches to disease control (англ.) // International Journal for Parasitology : journal. — Elsevier, 2005. — Vol. 35, no. 11—12. — P. 1169—1180. — doi:10.1016/j.ijpara.2005.07.001. (недоступная ссылка)
- Rose K. et al. Cutaneous leishmaniasis in red kangaroos: isolation and characterisation of the causative organisms (англ.) // International Journal for Parasitology : journal. — Elsevier, 2004. — Vol. 34, no. 6. — P. 655—664. — doi:10.1016/j.ijpara.2004.03.001. (недоступная ссылка)
- Momen H., Cupolillo E. Speculations on the origin and evolution of the genus Leishmania (англ.) // Memórias do Instituto Oswaldo Cruz : journal. — 2000. — Vol. 95, no. 4. — P. 583—588. — doi:10.1590/S0074-02762000000400023. — PMID 10904419.
- Noyes H.A., Morrison D.A., Chance M.L., Ellis J.T. Evidence for a neotropical origin of Leishmania (неопр.) // Memórias do Instituto Oswaldo Cruz. — 2000. — Т. 95, № 4. — С. 575—578. — doi:10.1590/S0074-02762000000400021. — PMID 10904417.
- Kerr S.F. Palaearctic origin of Leishmania (неопр.) // Memórias do Instituto Oswaldo Cruz. — 2000. — Т. 95, № 1. — С. 75—80. — doi:10.1590/S0074-02762000000100011. — PMID 10656708.
- Leishmania mexicana / Leishmania major (недоступная ссылка). Дата обращения: 1 февраля 2008. Архивировано 15 октября 2007 года.
- Faulde M. et al. Differences in transmission seasons as an epidemiological tool for characterization of anthroponotic and zoonotic cutaneous leishmaniasis in northern Afghanistan (англ.) // Acta Tropica : journal. — 2008. — Vol. 105, no. 2. — P. 131—138. (недоступная ссылка)
- Adler S. and Gunders A. E. Immunity to Leishmania mexicana following spontaneous recovery from oriental sore (англ.) // Transactions of the Royal Society of Tropical Medicine and Hygiene : journal. — 1964. — Vol. 58, no. 3. — P. 274—277. — doi:10.1016/0035-9203(64)90041-0. (недоступная ссылка)
- van Zandbergen G. et al. Leishmania disease development depends on the presence of apoptotic promastigotes in the virulent inoculum (англ.) // Proceedings of the National Academy of Sciences : journal. — United States National Academy of Sciences, 2006. — Vol. 103, no. 37. — P. 13837—13842. — doi:10.1073/pnas.0600843103. — PMID 16945916.
- Douba M. et al. Current status of cutaneous leishmaniasis in Aleppo, Syrian Arab Republic (англ.) // Bulletin of the World Health Organization : journal. — World Health Organization, 1997. — Vol. 75, no. 3. — P. 253—259. — PMID 9277013.
- Hoare C.A. Early discoveries regarding the parasite of oriental sore (англ.) // Transactions of the Royal Society of Tropical Medicine and Hygiene : journal. — 1938. — Vol. 32, no. 1. — P. 67—92. — doi:10.1016/S0035-9203(38)90097-5.
- Родякин Н. Ф., Суколин Г. И. Лейшманиоз кожный // Кожные и венерические болезни. Руководство для врачей / Ю. К. Скрипкин, В. Н. Мордовцев (ред.). — 2-е изд.. — М.: «Медицина», 1999. — Т. 1. — С. 394.
- Koževnikov P.V. Two nosological forms of cutaneous leishmaniasis (неопр.) // American Journal of Tropical Medicine and Hygiene. — 1963. — Т. 12, № 5. — С. 719—724. — PMID 14070762.
- Bray R. S. et al. The parasite causing cutaneous leishmaniasis in Ethiopia (англ.) // Transactions of the Royal Society of Tropical Medicine and Hygiene : journal. — 1973. — Vol. 67, no. 3. — P. 345—348. — doi:10.1016/0035-9203(73)90111-9. (недоступная ссылка)
- Bray R.S. Leishmania (неопр.) // Annual Review of Microbiology. — 1974. — Т. 28, № 1. — С. 189—217. — doi:10.1146/annurev.mi.28.100174.001201.
- da Fonseca F. Differentiation of flagellates of the genus Leishmania Ross, 1903, by the lytic action of specific sera (англ.) // American Journal of Tropical Medicine and Hygiene : journal. — 1933. — Vol. s1—13, no. 1. — P. 113—126.
- Schnur L. F. et al. Multifarious characterization of Leishmania tropica from a Judean desert focus, exposing intraspecific diversity and incriminating Phlebotomus sergenti as its vector (англ.) // American Journal of Tropical Medicine and Hygiene : journal. — 2004. — Vol. 70, no. 4. — P. 364—372.
- Gardener P.J. et al. Biochemical taxonomy of Leishmania. II: Electrophoretic variation of malate dehydrogenase (англ.) // Annals of Tropical Medicine and Parasitology : journal. — 1974. — Vol. 68, no. 3. — P. 317—325. — PMID 4447390.
- Gardener P.J. Taxonomy of the genus Leishmania: a review of nomenclature and classification (англ.) // Tropical Diseases Bulletin : journal. — 1977. — Vol. 74, no. 12. — P. 1069—1088. — PMID 345571.
- Chance M.L. et al. The identity of African rodent leishmanias (неопр.) // Transactions of the Royal Society of Tropical Medicine and Hygiene. — 1977. — Т. 71, № 2. — С. 109—117. — doi:10.1016/0035-9203(77)90073-6. (недоступная ссылка)
- Kreutzer R.D. and Christensen H.A. Characterization of Leishmania spp. by isozyme electrophoresis (англ.) // American Journal of Tropical Medicine and Hygiene : journal. — 1980. — Vol. 29, no. 2. — P. 199—208. — PMID 7369438.
- Université Montpellier 1. Identification des Leishmania. Laboratoire de Parasitologie-Mycologie. Дата обращения: 16 июля 2010. Архивировано 4 марта 2012 года.
- Piarroux R. et al. The use of isoelectric focusing on polyacrylamide gel for the enzymatic analysis of 'Old World' Leishmania species (англ.) // Transactions of the Royal Society of Tropical Medicine and Hygiene : journal. — 1994. — Vol. 88, no. 4. — P. 475—478. — doi:10.1016/0035-9203(94)90439-1. (недоступная ссылка)
- Schönian G. et al. Leishmaniases in the Mediterranean in the era of molecular epidemiology (англ.) // Trends in Parasitology : journal. — Cell Press, 2008. — Vol. 24, no. 3. — P. 135—142. — doi:10.1016/j.pt.2007.12.006. — PMID 18262469. (недоступная ссылка)
- Myler P; Fasel N (editors). Leishmania: After The Genome (неопр.). — Caister Academic Press, 2008.
- Akopyants N.S. et al. Demonstration of genetic exchange during cyclical development of Leishmania in the sand fly vector (англ.) // Science : journal. — 2009. — April (vol. 324, no. 5934). — P. 265—268. — doi:10.1126/science.1169464.
