Гепатит E
Вирусный гепати́т E (гепатит ни A ни B с фекально-оральным механизмом заражения) — острая циклическая вирусная инфекция с фекально-оральным механизмом заражения, склонная к эпидемическому распространению в основном в регионах с жарким климатом, протекающая преимущественно доброкачественно, но с большой частотой неблагоприятных исходов у женщин в последнем триместре беременности.
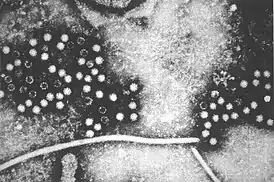
| Вирусный гепатит E | |
|---|---|
 | |
| МКБ-11 | 1E50.4 |
| МКБ-10 | B17.2 |
| МКБ-9 | 070.4 |
| DiseasesDB | 5794 |
| eMedicine | med/995 |
| MeSH | D016751 |
Этиология
Возбудитель — вирус гепатита E (HEV) относится к роду Hepevirus. Вирус имеет форму икосаэдра, оболочка отсутствует. Размер вирусных частиц составляет 32-34 нм, геном представлен однонитевой кодирующей РНК, длиной около 7,5 кб. Вирус относительно неустойчив во внешней среде, гибнет при кипячении, под действием антисептиков, однако может длительно сохраняться в пресной воде.
Выделяют пять генотипов HEV, изолированные в разных регионах — Азиатско-Африканском, Мексиканском и Североамериканском: 1 и 2 генотипы обнаруживаются исключительно у человека, 3 и 4 — зоонозные, выявляется у человека и теплокровных животных (кабан, олень), генотип 7 поражает преимущественно дромадеров.[1][2]
Эпидемиология
Заболевание чаще регистрируется в развивающихся странах вблизи экватора. Источник инфекции — больной человек, преимущественно в ранние сроки заболевания. Механизм передачи инфекции - орально-фекальный, преимущественно с водным путем заражения. Возможно инфицирование алиментарным путем при употреблении в пищу сырых моллюсков. Восприимчивость к вирусу всеобщая. Преимущественно заболевают взрослые в возрасте 15 - 50 лет, чаще мужчины. Ежегодно регистрируется около 20 млн случаев инфекции: 70 000 со смертельным исходом и 3 000 случаев мертворождения.[3] В эндемических регионах инфекция регистрируется постоянно. Пик заболеваемости приходится на дождливые сезоны, имеется связь с наводнениями и перенаселенностью.
Патогенез и патологическая анатомия
Основные звенья патогенеза идентичны гепатиту A. HEV обладает прямым цитопатическим действием и вызывает цитолиз гепатоцитов.
Морфологически выявляется фокальный, реже зональный некроз печени, у беременных женщин - массивный некроз печени.
Клиническая картина
Инкубационный период составляет от 20 до 65 дней. При своевременном иммунном ответе заболевание может протекать в субклинической и манифестной формах.Течение сходно с гепатитом A.
Заболевание можно разделить на две фазы: продромальный период и разгар заболевания.
Продромальный период длится 3 - 7 дней, сопровождается общей слабостью, диспепсическим синдромом, у 70 % больных наблюдается выраженный болевой синдром, проявляющийся еще в преджелтушный период и проявляющийся миалгией, артралгией и болями в эпигастрии. Возможно повышение температуры тела. К концу преджелтушного периода повышается активность аланинаминотрансферазы и аспартатаминотрансферазы, DRr≤1, иногда до 20-кратного предела верхней нормы, достигая пика к 5 неделе от начала заболевания. Наблюдается незначительное повышение активности щелочной фосфатазы. Уровень билирубина в сыворотке колеблется от 85 до 342 мкмоль/л, в зависимости от степени поражения гепатоцитов. В периферической крови определяется лейкопения с нейтропенией или лимфопенией. В разгар заболевания, при появлении желтухи, состояние больных не улучшается. Желтуха и интоксикация кратковременны. Закономерно увеличение печени и редко (в отличие от гепатита A) спленомегалия. Моча имеет темную окраску, стул слабоокрашен. Заболевание протекает, как правило, в формах легкой и средней тяжести. Общая длительность клинических проявлений 14 - 25 дней.
Длительное вирусоносительство не развивается. Хронизация гепатита и быстрое развитие фиброза печени[4] наблюдается у реципиентов органов[5], у инфицированных вирусом иммунодефицита человека (ВИЧ)[6][7], у пациентов получающих лечение ритуксимабом при неходжкинской лимфоме[8].
Восстановительный период более длительный, чем при гепатите A.
Диагностика
Диагностика основана на клинико-эпидемиологических данных с учетом географического анамнеза при исключении гепатитов A, B, C. Диагноз подтверждается обнаружением методом ИФА в крови анти-HEV-IgM[9], который появляется к 10 дню заболевания и выявляется в течение 1 - 2 месяцев.[10] В ранние сроки возможна индикация РНК HEV в фекалиях и крови методом ПЦР, ELISA[11] или иммунофлюоресцентное обнаружение вируса в фекалиях и биопате печени.[12]
Лечение
Лечение симптоматическое, аналогично таковому при гепатите A. В случае тяжелого течения инфекции рекомендуется рибавирин.[13] Беременные женщины нуждаются в госпитализации. Акушерская тактика сводится к сохранению беременности. Искусственное прерывание возможно только в период рековалесценции. Назначение рибавирина беременным не рекомендуется, в связи с его выраженным тератогенным эффектом.[10]
Прогноз
Инфекция оканчивается выздоровлением. Летальность составляет 4%. Среди беременных женщин уровень достигает 20%, этот показатель увеличивается во втором и третьем триместрах. Сообщаемые причины смерти включают энцефалопатию и диссеминированное внутрисосудистое свертывание. Уровень молниеносной печеночной недостаточности у инфицированных беременных женщин высок.
Профилактика
Заключается преимущественно в соблюдении санитарно-гигиенических норм. Путешественникам не следует употреблять сырую воду в странах, где регистрируется гепатит E.
Также разработана рекомбинантная вакцина, показавшая высокую эффективность в клинических испытаниях[14][15].
Примечания
- Mushahwar IK. Hepatitis E virus: molecular virology, clinical features, diagnosis, transmission, epidemiology, and prevention. // J Med Virol. 2008; 80(4):646-58 (ISSN: 0146-6615).
- Khuroo MS; Khuroo MS; Khuroo NS. Transmission of Hepatitis E Virus in Developing Countries. // Viruses. 2016; 8(9) (ISSN: 1999-4915).
- Rein DB; Stevens GA; Theaker J; Wittenborn JS; Wiersma ST. The global burden of hepatitis E virus genotypes 1 and 2 in 2005. // Hepatology. 2012; 55(4):988-97 (ISSN: 1527-3350).
- Behrendt P; Steinmann E; Manns MP; Wedemeyer H. The impact of hepatitis E in the liver transplant setting. // J Hepatol. 2014; 61(6):1418-29 (ISSN: 1600-0641).
- Kamar N; Selves J; Mansuy JM; Ouezzani L; Péron JM; Guitard J; Cointault O; Esposito L; Abravanel F; Danjoux M; Durand D; Vinel JP; Izopet J; Rostaing L. Hepatitis E virus and chronic hepatitis in organ-transplant recipients. // N Engl J Med. 2008; 358(8):811-7 (ISSN: 1533-4406).
- Dalton HR; Bendall RP; Keane FE; Tedder RS; Ijaz S. Persistent carriage of hepatitis E virus in patients with HIV infection. // N Engl J Med. 2009; 361(10):1025-7 (ISSN: 1533-4406).
- Puoti M; Moioli MC; Travi G; Rossotti R. The burden of liver disease in human immunodeficiency virus-infected patients. // Semin Liver Dis. 2012; 32(2):103-13 (ISSN: 1098-8971).
- Ollier L; Tieulie N; Sanderson F; Heudier P; Giordanengo V; Fuzibet JG; Nicand E. Chronic hepatitis after hepatitis E virus infection in a patient with non-Hodgkin lymphoma taking rituximab. // Ann Intern Med. 2009; 150(6):430-1 (ISSN: 1539-3704).
- Legrand-Abravanel F; Thevenet I; Mansuy JM; Saune K; Vischi F; Peron JM; Kamar N; Rostaing L; Izopet J. Good performance of immunoglobulin M assays in diagnosing genotype 3 hepatitis E virus infections. // Clin Vaccine Immunol. 2009; 16(5):772-4 (ISSN: 1556-679X).
- Kamar N; Bendall R; Legrand-Abravanel F; Xia NS; Ijaz S; Izopet J; Dalton HR. Hepatitis E. // Lancet. 2012; 379(9835):2477-2488 (ISSN: 1474-547X).
- Chionne P; Madonna E; Pisani G; Taffon S; La Rosa G; Candido A; Dettori S; Tritarelli E; Equestre M; Bruni R; Ciccaglione AR. Evaluation of rapid tests for diagnosis of acute hepatitis E. // J Clin Virol. 2016; 78:4-8 (ISSN: 1873-5967).
- Clayson ET; Myint KS; Snitbhan R; Vaughn DW; Innis BL; Chan L; Cheung P; Shrestha MP. Viremia, fecal shedding, and IgM and IgG responses in patients with hepatitis E. // J Infect Dis. 1995; 172(4):927-33 (ISSN: 0022-1899).
- Gerolami R; Borentain P; Raissouni F; Motte A; Solas C; Colson P. Treatment of severe acute hepatitis E by ribavirin. // J Clin Virol. 2011; 52(1):60-2 (ISSN: 1873-5967).
- Shrestha MP; Scott RM; Joshi DM; Mammen MP; Thapa GB; Thapa N; Myint KS; Fourneau M; Kuschner RA; Shrestha SK; David MP; Seriwatana J; Vaughn DW; Safary A; Endy TP; Innis BL. Safety and efficacy of a recombinant hepatitis E vaccine. // N Engl J Med. 2007; 356(9):895-903 (ISSN: 1533-4406).
- TheLancet.com - Maintenance
Литература
- http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(10)61393-1/fulltext
- Инфекционные болезни с курсом паразитологии: в 3 т./Под ред. Ж. И. Возиановой - Киïв "Здоров'я", 2002 - ISBN 5-311-01296-X
- Тропические болезни/Под ред. Е. П. Шуваловой - СПб Издательство "ЭЛБИ-СПб", 2004 - ISBN 5-93979-102-6
- https://emedicine.medscape.com/article/178140-overview
