Вентролатеральное преоптическое ядро
Вентролатеральное преоптическое ядро (англ. Ventrolateral preoptic nucleus, VLPO; другие варианты перевода — вентролатеральное ядро преоптической области, вентролатеральная преоптическая область) — небольшой участок нейронов в переднем ядре гипоталамуса, расположенный над перекрёстом зрительных нервов в головном мозге человека и животных[1]. Один из центров сна головного мозга (куда также входят парафациальная зона продолговатого мозга, прилежащее ядро и нейроны меланин-концентрирующего гормона латеральной области гипоталамуса)[2][3][4][5][6]. Вместе с восходящей активизирующей ретикулярной системой и системой орексинных аксонов латерального гипоталамуса образует связанную систему нейронов, контролирующих состояния бодрствования, сна, а также переходы между двумя этими состояниями[1][3][4]. Вентролатеральное преоптическое ядро активизируется в процессе сна (в основном в ходе медленного сна, NREM-сон), и выделяет тормозные нейромедиаторы, в основном ГАМК и галанин, которые ингибируют нейроны восходящей активизирующей ретикулярной формации, отвечающие за поддержание бодрствования[1]. Активизация вентролатерального преоптического ядра осуществляется нейромедиаторами серотонином и аденозином[7], а также простагландином D2[8]. Ингибирование вентролатерального преоптического ядра осуществляется нейромедиаторами норадреналином и ацетилхолином[9]. Изучение данной области и её значение в регулировании сна и бодрствования, включая нарушения сна, является предметом повышенного интереса у нейробиологов.
| Ventrolateral Preoptic Nucleus | |
|---|---|
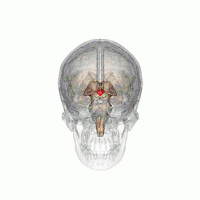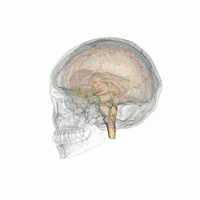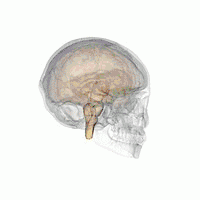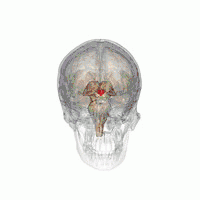 Вентролатеральное преоптическое ядро (VLPO) расположено в переднем ядре гипоталамуса | |
| Часть | Преоптическое ядро |
| Сокращение | VLPO |
Структура
Около 80 % нейронов вентролатерального преоптического ядра являются ГАМК-эргическими (тормозными нейронами, использующими в качестве нейромедиатора гамма-аминомасляную кислоту)[10].
Эксперименты на крысах продемонстрировали, что две трети вентролатерального преоптического ядра состоит из гомогенных мультиполярных нейронов треугольной формы с низкопороговыми кальциевыми каналами[11].
Около двух третей нейронов в этой области активируются во время сна. Ингибирирование активности мультиполярных нейронов данной области происходит при помощи норадреналина и ацетилхолина. Известно два типа мультиполярных нейронов вентролатерального ядра преоптической области:
- Тип 1 — ингибируются серотонином.
- Тип 2 — возбуждаются серотонином, а также аденозином.
Известно, что концентрация серотонина и аденозина возрастает во время бодрствования, поэтому, вероятно, нейроны типа 2 играют роль в засыпании, а нейроны типа 1 — в консолидации сна[7].
Передача возбуждения в оставшейся трети нейронов вентролатерального преоптического ядра осуществляется посредством норадреналина. Их роль остаётся неизученной.
Функции
Сон и бодрствование
Ещё в середине XX века было обнаружено, что повреждения вентролатерального преоптического ядра у крыс и кошек вызывает бессонницу[12][13], что подтвердило ключевую роль ядра в регулировании сна. Вентролатеральное преоптическое ядро иннервирует клеточные тела и проксимальные дендриты областей мозга, которые отвечают за состояние бодрствования: туберомамиллярное ядро (TMN), ядра шва, голубое пятно, педункулопонтийное тегментальное ядро, латеродорсальное тегментальное ядро, чёрную субстанцию, околоводопроводное серое вещество и орексинные нейроны. Все эти ядра и области входят в так называемую диффузную модуляторную систему (DMS).
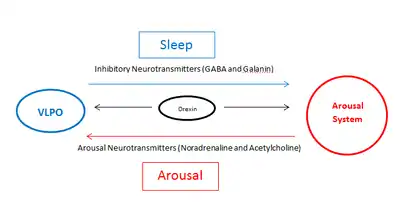
Вентролатеральное преоптическое ядро активизируется серотонином, аденозином и простагландином D2, концентрация которых повышается во время бодрствования. Большинство нейронов ядра VLPO являются ГАМК-эргическими и галанин-эргическими, то есть секретирующими тормозные нейромедиаторы ГАМК и галанин соответственно. Секреция этих тормозных медиаторов подавляет систему бодрствования и вызывает сон. Вентролатеральное преоптическое ядро также получает восходящие проекции из диффузной модуляторной системы, отвечающей за бодрствование. Эти восходящие проекции ретикулярной формации секретируют нейромедиаторы норадреналин и ацетилхолин, которые тормозят вентролатеральное преоптическое ядро и вызывают пробуждение и бодрствование. Активность вентролатерального преоптического ядра обратно пропорциональна активности системы бодрствования (при активизации вентролатеральной преоптической области активность системы бодрствования снижается, и наоборот).
Одной из теорий, объясняющих функционирование вентролатерального преоптического ядра, является гипотеза «выключателя» (англ. Flip-Flop Switch Hypothesis)[14]. Согласно данной гипотезе, вентролатеральное преоптическое ядро и систему бодрствования можно представить в качестве двух положений «переключателя»; в конкретный момент времени активной может быть только одна из этих систем, «переключая» мозг в состояние сна или бодрствования соответственно. Орексинные нейроны заднего отдела гипоталамуса возбуждают ядра мозговой «системы бодрствования», а также, вероятно, ингибируют активность вентролатерального преоптического ядра[14]. Таким образом, орексинные нейроны играют существенную роль в «переключении» состояний сна и бодрствования.
Циркадные ритмы
Сон тесно связан с циркадными ритмами. У млекопитающих регулирование циркадных ритмов осуществляет супрахиазматическое ядро гипоталамуса, небольшое количество проводящих путей из которого идёт в вентролатеральное преоптическое ядро. Как считается, эти пути активируют ГАМК-эргические нейроны вентролатерального преоптического ядра, что инициирует начало сна[14]. Из вентролатерального преоптического ядра также отходят пути в супрахиазматическое ядро; это может означать, что вентролатеральное преоптическое ядро также оказывает влияние на циркадные ритмы млекопитающих.
Клиническое значение
Бессонница
Люди преклонного возраста с большим количеством галаниновых нейронов в вентролатеральном ядре имеют продолжительный, качественный сон, тогда как снижение количества этих нейронов связывают с фрагментированным сном (больше пробуждений посреди ночи)[15][16].
Повреждения вентролатерального преоптического ядра у крыс вызывает снижение длительности медленного сна (NREM-сон) на 50—60 % и вызывает продолжительную бессонницу[17]. Вероятно, нарушения работы вентролатерального преоптического ядра вызывают недостаточно регулярное и слабое торможение системы бодрствования, что приводит к частым ночным пробуждениям пациентов с бессонницей[18].
Нарколепсия
Нарколепсия типа I ассоциируется с недостатком орексинов, что приводит к нарушениям нормальных «переключений» между вентролатеральным преоптическим ядром и системой бодрствования, включая приступы внезапного дневного засыпания и нарушения ночного сна[14].
Глубокая стимуляция головного мозга
В 2013 году был протестирован метод глубокой стимуляции мозга посредством «проектора магнитного поля» (англ. Magnetic Field Projector). Данный метод, использованный на крысах, продемонстрировал активизацию нейронов вентролатерального преоптического ядра и вызвал сон[19]. Этот новый метод глубокой стимуляции мозга не требует хирургических вмешательств и гораздо дешевле, чем ранее применявшиеся методики, однако на людях он ещё не тестировался.
Примечания
- Malenka RC, Nestler EJ, Hyman SE. Molecular Neuropharmacology: A Foundation for Clinical Neuroscience. — 2nd. — New York: McGraw-Hill Medical, 2009. — P. 294–296. — ISBN 9780071481274.
- Anaclet C., Ferrari L., Arrigoni E., Bass C. E., Saper C. B., Lu J., Fuller P. M. The GABAergic parafacial zone is a medullary slow wave sleep-promoting center (англ.) // Nat. Neurosci. : journal. — 2014. — September (vol. 17, no. 9). — P. 1217—1224. — doi:10.1038/nn.3789. — PMID 25129078.
- Schwartz M. D., Kilduff T. S. The Neurobiology of Sleep and Wakefulness (англ.) // The Psychiatric Clinics of North America : journal. — 2015. — December (vol. 38, no. 4). — P. 615—644. — doi:10.1016/j.psc.2015.07.002. — PMID 26600100.
- Brown R. E., McKenna J. T. Turning a Negative into a Positive: Ascending GABAergic Control of Cortical Activation and Arousal (англ.) // Front. Neurol. : journal. — 2015. — June (vol. 6). — P. 135. — doi:10.3389/fneur.2015.00135. — PMID 26124745.
- Valencia Garcia S., Fort P. Nucleus Accumbens, a new sleep-regulating area through the integration of motivational stimuli (англ.) // Acta Pharmacologica Sinica : journal. — 2017. — December. — doi:10.1038/aps.2017.168. — PMID 29283174.
- Oishi Y., Xu Q., Wang L., Zhang B. J., Takahashi K., Takata Y., Luo Y. J., Cherasse Y., Schiffmann S. N., de Kerchove d'Exaerde A., Urade Y., Qu W. M., Huang Z. L., Lazarus M. Slow-wave sleep is controlled by a subset of nucleus accumbens core neurons in mice (англ.) // Nature Communications : journal. — Nature Publishing Group, 2017. — September (vol. 8, no. 1). — P. 734. — doi:10.1038/s41467-017-00781-4. — PMID 28963505.
- Gallopin T. The endogenous somnogen adenosine excites a subset of sleep-promoting neurons via A2A receptors in the ventrolateral preoptic nucleus (англ.) // Neuroscience : journal. — Elsevier, 2005. — Vol. 134, no. 4. — P. 1377—1390. — doi:10.1016/j.neuroscience.2005.05.045. — PMID 16039802.
- Scammell T. Activation of ventrolateral preoptic neurons by the somnogen prostaglandin D2 (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 1998. — Vol. 95. — P. 7754—7759. — doi:10.1073/pnas.95.13.7754.
- Chou T. Afferents to the Ventrolateral Preoptic Nucleus (англ.) // The Journal of Neuroscience : journal. — 2002. — Vol. 22. — P. 977—990.
- Sherin J. Innervation of Histaminergic Tuberomammillary Neurons by GABAergic and Galaninergic Neurons in the Ventrolateral Preoptic Nucleus of the Rat (англ.) // The Journal of Neuroscience : journal. — 1998. — Vol. 18, no. 12. — P. 4705—4721.
- Gallopin T. Identification of sleep-promoting neurons in vitro (англ.) // Nature : journal. — 2000. — Vol. 404. — P. 992—995. — doi:10.1038/35010109.
- Nauta W. Hypothalamic regulation of sleep in rats (англ.) // Journal of Neurophysiology : journal. — 1946. — Vol. 9. — P. 285—314.
- McGinty D. Sleep Suppression after Basal Forebrain Lesions in the Cat (англ.) // Science : journal. — 1968. — Vol. 160, no. 3833. — P. 1253—1255. — doi:10.1126/science.160.3833.1253.
- Saper C. Hypothalamic regulation of sleep and circadian rhythms (англ.) // Nature : journal. — 2005. — Vol. 437, no. 7063. — P. 1257—1263. — doi:10.1038/nature04284. — PMID 16251950.
- Lim A. Sleep is related to neuron numbers in the ventrolateral preoptic/intermediate nucleus in older adults with and without Alzheimer’s disease (англ.) // Brain : journal. — Oxford University Press, 2014. — Vol. 137. — P. 2847—2861.
- Ученые нашли причину бессонницы у пожилых людей. Lenta.ru (20 августа 2014).
- Liu J. Selective activation of the extended ventrolateral preoptic nucleus during rapid eye movement sleep (англ.) // The Journal of Neuroscience : journal. — 2002. — Vol. 22. — P. 4568—4576.
- Winrow C. Discovery and development of orexin receptor antagonists as therapeutics for insomnia (англ.) // British Journal of Pharmacology : journal. — 2014. — Vol. 171. — P. 283—293. — doi:10.1111/bph.12261.
- Jie F. A magnetic field projector for deep brain modulation (англ.) // Neural Engineering : journal. — 2013. — P. 1214—1217. — doi:10.1109/NER.2013.6696158.
- Moore J. Direct Activation of Sleep-Promoting VLPO Neurons by Volatile Anesthetics Contributes to Anesthetic Hypnosis (англ.) // Current Biology : journal. — Cell Press, 2012. — Vol. 22. — P. 2008—2016. — doi:10.1016/j.cub.2012.08.042.
- Liu Y. Propofol Facilitates Glutamatergic Transmission to Neurons of the Ventrolateral Preoptic Nucleus (англ.) // Anesthesiology : journal. — Lippincott Williams & Wilkins, 2013. — Vol. 111. — P. 1271—1278.. — doi:10.1097/ALN.0b013e3181bf1d79.
Ссылки
- ancil--1174961713 на сайте NeuroNames (англ.)
- Статья на сайте Science Direct (англ.)
- Gaus SE, Strecker RE, Tate BA, Parker RA, Saper CB. Ventrolateral preoptic nucleus contains sleep-active, galaninergic neurons in multiple mammalian species : [англ.] // Neuroscience. — 2002. — № 115. — С. 85—94.
- Gallopin T., Luppi P. H., Cauli B., Urade Y., Rossier J., Hayaishi O., Lambolez B., Fort P. The endogenous somnogen adenosine excites a subset of sleep-promoting neurons via A2A receptors in the ventrolateral preoptic nucleus (англ.) // Neuroscience : journal. — Elsevier, 2005. — Vol. 134, no. 4. — P. 1377—1390. — doi:10.1016/j.neuroscience.2005.05.045. — PMID 16039802. (англ.)