Азооспермия
Азоосперми́я (от др.-греч. ἀ- — отсутствие, ζῷον — животное и σπέρμα — семя) — патологическое состояние, при котором в эякуляте отсутствуют сперматозоиды.
| Азооспермия | |
|---|---|
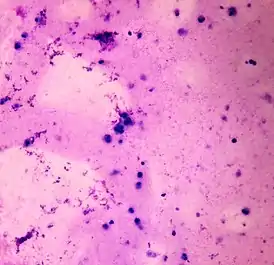 Анализ спермы не выявил сперматозоидов и множественных лейкоцитов | |
| МКБ-11 | GB04.0 |
| МКБ-10 | N46 |
| МКБ-10-КМ | N46.0 и N46.01 |
| МКБ-9 | 606.0 |
| МКБ-9-КМ | 606.0[1] |
| MeSH | D053713 |
Азооспермия является одной из причин мужского бесплодия. Азооспермию устанавливают с помощью анализа эякулята (спермограмма).
Различают необструктивную (секреторную) азооспермию, при которой в яичках не формируются сперматозоиды, и обструктивную (экскреторную) азооспермию, при которой сперматозоиды не попадают в эякулят из-за непроходимости семявыводящих путей. Возможна также сочетанная азооспермия, связанная одновременно с гипофункцией яичек и нарушением проходимости семявыводящих путей. Обструктивная азооспермия (экскреторное бесплодие) значительно лучше поддаётся лечению.
Факторами риска азооспермии являются генетические нарушения, токсические воздействия (включая алкоголь, химические вещества, радиационное облучение), воспалительные заболевания половых органов, приводящие к нарушению проходимости семявыносящих протоков, переохлаждение, авитаминоз.
Анализы при азооспермии
- Спермограмма
- Генитография
- Биопсия тканей яичек или придатков яичек.
- Анализ делеций AZF-локуса, который определяет, имеет ли бесплодие наследственные причины развития.
Гены
Азооспермия в брюшной полости может быть вызвана конгенсативным гипопитуитаризмом, синдромом Каллмана, синдромом Прадера-Вилли и другими генетическими состояниями, которые приводят к дефициту GnRH или гонадотропина. Азооспермия яичек проявляется при синдроме Клайнфелтера (XXY). Кроме того, у 13% мужчин с азооспермией имеется дефектный сперматогенез, связанный с дефектами Y-хромосомы. Такие дефекты, как правило, являются новыми микро-делециями и обычно затрагивают длинную руку хромосомы. Секция длинного плеча Y-хромосомы была названа Азооспермиевым фактором (AZF). Дефекты в этой области могут привести к олигоспермии или азооспермии, однако плотная корреляция генотипа и фенотипа не была достигнута.
Диагностика
Азооспермия обычно обнаруживается в ходе исследования бесплодия. Он устанавливается на основе двух оценок анализа спермы, проводимых в отдельных случаях (когда семенный образец после центрифугирования не показывает спермы под микроскопом) и требует дополнительной обработки. [2]
Исследование включает в себя историю, физический осмотр, включая тщательную оценку мошонки и яичек, лабораторные анализы и, в некоторых случаях, визуализацию. Диагностика включает общее состояние здоровья, сексуальное здоровье, прошлую плодовитость, либидо и сексуальную активность. Необходимо выявить историю ряда агентов, включая медицинские агенты, такие как терапия гормонами / стероидами, антибиотики, ингибиторы 5-ASA (сульфасалазин), альфа-блокаторы, ингибиторы 5 альфа-редуктазы, химиотерапевтические агенты, пестициды, рекреационные наркотики (марихуана, чрезмерный алкоголь) и тепловое воздействие яичек. Необходимо выявить историю хирургических процедур генитальной системы. Необходимо изучить семейную историю, чтобы искать генетические аномалии.
Врожденное отсутствие семявыносящего протока может быть обнаружено при физическом обследовании и может быть подтверждено трансректальным ультразвуком (ТРУЗИ). Если подтвержденное генетическое тестирование на кистозный фиброз. Трансректальное ультразвуковое исследование также может оценивать азооспермию, вызванную обструкцией, или аномалии, связанные с обструкцией эякуляторного канала, такие как аномалии внутри самого канала, медианная киста предстательной железы (указывающая на необходимость аспирации кисты) или нарушение семенных пузырьков. Ретроградная эякуляция диагностируется путем изучения постэякуляторной мочи на наличие спермы после ее щелочного анализа и центрифугирования. [3]
Низкие уровни лютеинизирующих гормонов и фолликулостимулирующих гормонов с низким или нормальным уровнем тестостерона свидетельствуют о протестикулярных проблемах, в то время как высокий уровень гонадотропинов указывает на проблемы с тестикулами. Однако часто это различие не ясны, и дифференциация между обструктивной и неинъекционной азооспермией может потребовать биопсии яичка. С другой стороны, у азооспермических мужчин с нормальным объемом эякулята уровень сыворотки фолликулостимулирующих гормонов, превышающий в два раза верхний предел нормального диапазона, достоверно диагностирует дисфункциональный сперматогенез, и, когда его обнаруживают, диагностическая биопсия яичка обычно не нужна. Также, чрезвычайно высокие уровни фолликулостимулирующих гормонов (> 45 ID / мл) должны быть сопоставлены с успешной экстракцией микродиссекции яичек. [4]
Ингибин-В сыворотки слабо указывают на присутствие сперматозоидов в семенниках, при этом шансы на оценку успешного оплодотворения достигаются путем экстракции семенников яичек. В Mount Sinai Hospital, Канада, в 2016 году были предложены семенные плазменные белки TEX101 и ECM1 для дифференциальной диагностики форм и подтипов азооспермии и для прогнозирования результатов экстракции семенников яичек, начаты клинические испытания по их проверке.
Рекомендуется, чтобы у мужчин первичный гипопитуитаризм был связан с генетическими оценками; азооспермическим мужчинам с тестикулярной недостаточностью рекомендуется пройти кариотип и Y-микро-удаление.[5][6][2]
Лечение
Предварительная и послестерическая азооспермия часто являются правильными, в случае если азооспермия яичек является постоянной. В первом случае необходимо рассмотреть причину азооспермии, в дальнейшем это открывает возможности для непосредственного управления ситуацией. Таким образом, мужчины с азооспермией из-за гиперпролактинемии могут возобновить производство спермы после лечения гиперпролактинемии; мужчины, чья продукция спермы подавляется экзогенными андрогенами, как ожидается, будет производить сперму после прекращения приема андрогена. В ситуациях, когда яички являются нормальными, но не стимулированными, можно ожидать, что терапия гонадотропином вызовет выработку спермы.
Значительным достижением в последние годы стало внедрение экстракорпорального оплодотворения с ИКСИ, которое позволяет успешно оплодотворить даже с незрелой спермой или спермой, полученной непосредственно из ткани яичка. Оба метода предполагают беременность в парах, где у человека есть необратимая азооспермия яичек, если можно извлечь из семен семени материал спермы. Таким образом, у мужчин с немозаичным синдромом Клайнфелтера могут родиться дети. Бывали случаи, когда беременность была достигнута в ситуациях, при которых азооспермия ассоциировалась с крипторхизмом и спермой, где была получена экстракция семенниками яичек (TESE). Лекарства могут быть полезны от преждевременной эякуляции.
Примечания
- база данных Disease ontology (англ.) — 2016.
- Esteves SC, Miyaoka R, Agarwal A. An update on the clinical assessment of the infertile male. Clinics (Sao Paulo). [corrected]. 2011;66(4):691–700.
- Lotti, F.; Maggi, M. Ultrasound of the male genital tract in relation to male reproductive health (англ.) // Human Reproduction : journal. — 2014. — Vol. 21, no. 1. — P. 56—83. — ISSN 1355-4786. — doi:10.1093/humupd/dmu042. — PMID 25038770.
- Ramasamy R, Lin K, Gosden LV, Rosenwaks Z, Palermo GD, Schlegel PN. High serum FSH levels in men with nonobstructive azoospermia does not affect success of microdissection testicular sperm extraction. Fertil Steril. 2009;92(2):590-3.
- Schlegel, P.N. Causes of azoospermia and their management (неопр.) // Reproduction, fertility, and development. — 2004. — Т. 16, № 5. — С. 561—572. — doi:10.1071/RD03087. — PMID 15367371.
- Poongothai, J; Gopenath, TS; Manonayaki, S. Genetics of human male infertility (неопр.) // Singapore medical journal. — 2009. — Т. 50, № 4. — С. 336—347. — PMID 19421675.