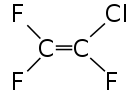
1,1,2-Трифтор-2-хлорэтилен
1,1,2-Трифтор-2-хлорэтилен — относится к фторолефинам — алкенам, в которых один или несколько атомов водорода замещены атомами фтора. Является непредельным фторорганическим соединением и служит в качестве мономера (Мономер-3) для производства фторкаучука СКФ-32 — сополимера с Мономером-2.
| 1,1,2-Трифтор-2-хлорэтилен | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
1,1,2-Трифтор-2-хлорэтилен | ||
| Традиционные названия |
Трифторхлорэтилен, Перфторвинилхлорид, Мономер-3 (М-3), Хлортрифторэтилен, Трифторвинилхлорид |
||
| Хим. формула | C2F3Cl | ||
| Рац. формула | CF2CFCl | ||
| Физические свойства | |||
| Состояние | бесцветный газ | ||
| Молярная масса | 116,47 г/моль | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -157,9 °C | ||
| • кипения | -26,8 °C | ||
| Критическая точка |
температура: 106,2 °C давление: 4,07 МПа плотность: |
||
| Химические свойства | |||
| Растворимость | |||
| • в воде | 0 г/100 мл | ||
| Классификация | |||
| Рег. номер CAS | 79-38-9 | ||
| PubChem | 6594 | ||
| Рег. номер EINECS | 201-201-8 | ||
| SMILES | |||
| InChI | |||
| ChemSpider | 6345 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Свойства
Физические свойства
Бесцветный газ. Очень плохо растворим в воде, и хорошо — в органических растворителях. Сильно токсичное вещество, все работы с которым проводятся с эффективной вентиляцией. В расплаве имеет высокую вязкость, поэтому трудно перерабатывается литьём под давлением. С воздухом в концентрации 28,5—35,2 % образует взрывоопасные смеси.
Хранят в стальных баллонах; для предупреждения самопроизвольной полимеризации вводят ингибиторы (1 %) — трибутиламин или дипентен.
Химические свойства
Мономер-3 сравнительно легко полимеризуется при повышенной температуре и умеренном давлении в присутствии перекисных катализаторов. Под влиянием других инициаторов радикальных реакций, например облучения, образуется полимер с более высоким молекулярным весом. При хранении газообразного мономера на свету часто наблюдается медленная самопроизвольная полимеризация. Основным промышленным способом получения политрифторхлорэтилена является водно-эмульсионная полимеризация в присутствии персульфата аммония или калия, а также перекиси бария или цинка.[1].
Трифторхлорэтилен легко гидролизуется водой и взаимодействует с кислородом воздуха, особенно в присутствии воды.
Получение
Трифторхлорэтилен можно получать пиролитическим дегидрохлорированием 1,1,2-Трифтор-2,2-дихлорэтана на контакте, в качестве которого используют битое стекло, при температуре 560—575 °С[2]:
Другая реакция основана на дегалогенировании 1,1,2-Трифтор-1,2,2-трихлорэтана порошкообразным цинком в среде кипящего абсолютного спирта:
Вместо спирта можно применять безводный диоксан, глицерин или целлозольв.
Применение
Применяется, главным образом, для производства политрифторхлорэтилена (сополимера мономера-3 с мономером-2), а также как охладитель в производственных процессах при низкой температуре.
См. также
Ссылки
- Химический энциклопедический словарь / гл.ред. И.Л.Кнунянц. — М.: Сов. энциклопедия, 1983. — С. 638. — 792 с.
Примечания
- Трифторхлорэтилен. Информационный ресурс «Большая Энциклопедия Нефти Газа».
- Образование и получение трифторхлорэтилена. Информационный ресурс «Zomber.ru».