Эффект Джоуля — Томсона
Эффе́ктом Джо́уля — То́мсона называют изменение температуры газа или жидкости при стационарном адиабатическом дросселировании[1] — медленном протекании газа под действием постоянного перепада давлений сквозь дроссель (пористую перегородку). Назван в честь открывших его Джеймса Джоуля и Уильяма Томсона[K 1]. Данный эффект является одним из методов получения низких температур.
С именами Джоуля и Гей-Люссака связан несколько отличающийся по постановке эксперимента эффект: расширение газа через открытый клапан из сосуда высокого давления в сосуд с низким давлением (адиабатическое расширение в вакуум). Теория этого процесса к тому же имеет много сходных черт с анализом собственно эффекта Джоуля — Томсона, поэтому часто (в том числе и в настоящей статье) оба явления обсуждаются одновременно.
Процессы адиабатического расширения
Адиабатическое (в отсутствие теплообмена) и при этом стационарное (когда кинетическая энергия движения пренебрежимо мала) расширение может быть осуществлено различными способами. Изменение температуры при расширении зависит не только от начального и конечного давления, но и способа, которым осуществляется расширение.
- Обратимое расширение имеет место, если теплоизолированная термодинамическая система находится в термодинамическом равновесии в ходе процесса. Такое расширение называется изоэнтропийным, поскольку энтропия системы остаётся неизменной: . Обычным примером такого расширения является медленное расширение газа при движении закрывающего сосуд поршня. В этом случае при расширении, то есть при положительном изменении объёма система совершает положительную работу , где — давление. Как результат, внутренняя энергия уменьшается: [2].
- В процессе свободного расширения газ не совершает работу и не поглощает тепло, поэтому его внутренняя энергия сохраняется. При таком расширении, температура идеального газа оставалась бы постоянной, но температура реального газа может и уменьшаться[3].
- Метод расширения, описанный в настоящей статье как процесс Джоуля — Томсона, в которой газ или жидкость при давлении Р1 перетекает в область пониженного давления P2 без существенного изменения кинетической энергии, называется расширением Джоуля–Томсона. Расширение существенно необратимо. В ходе этого процесса энтальпия остается неизменной (см. доказательство ниже). В отличие от свободного расширения, совершается работа, вызывающая изменение внутренней энергии газа.
Термодинамика процесса Джоуля — Томсона
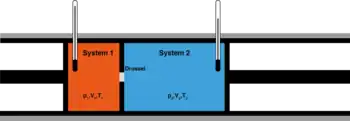
Эффект Джоуля — Томсона — это изоэнтальпийный процесс, что позволяет описать его методами термодинамики. Схема процесса представлена на рисунке 1. Левый поршень, вытесняя газ под давлением из объёма , совершает над ним работу . Пройдя через дроссель и расширяясь в объём , газ совершает работу над правым поршнем. Суммарная работа , совершенная над газом, равна изменению его внутренней энергии , так что энтальпия сохраняется: [4][5]
Изменение температуры
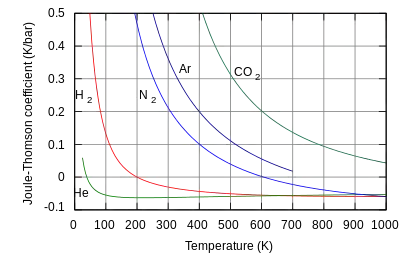
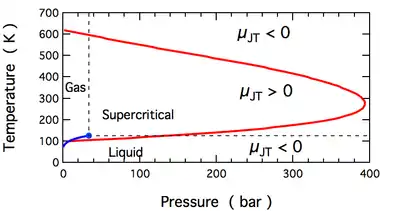
Сохранение энтальпии позволяет найти связь между изменениями давления и температуры в процессе Джоуля — Томсона. Чтобы установить эту связь, энтальпия должна быть выражена в виде функции от давления и температуры .
Чтобы получить выражение для дифференциала энтальпии в переменных дифференциал энтропии выражается через :
Температурная производная энтропии выражается через (измеримую) теплоёмкость при постоянном давлении . Производная энтропии по давлению выражаются с помощью четвёртого соотношения Максвелла (G2) что даёт и:
Изменение температуры при малом изменении давления (дифференциальный эффект) в результате процесса Джоуля — Томсона определяется производной , называемой коэффициентом Джоуля — Томсона.
Из уравнения для дифференциала энтальпии в переменных температура — давления находится связь между дифференциалами температуры и давления в изоэнтальпийном процессе (при ). Равенство нулю дифференциала энтальпии даёт[6][7] и
Для идеального газа , а для реального газа он определяется уравнением состояния.
Если при протекании газа через пористую перегородку температура возрастает (), то эффект называют отрицательным, и наоборот, если температура убывает (), то процесс называют положительным. Температуру, при которой меняет знак, называют температурой инверсии.
Применение
- Процесс Джоуля — Томсона используют для получения низких температур. Для этой цели обычно применяют интегральный процесс, при котором давление изменяется в широких пределах.
- Измерение позволяет установить уравнение состояния газа.
См. также
Комментарии
- Поскольку Томсон также известен под именем лорда Кельвина, в англоязычной литературе в названии эффекта может присутствовать имя Кельвина вместо Томсона
Примечания
- Зубарев Д. Н. Джоуля — Томсона эффект, 1988.
- Сивухин Д. В., Термодинамика и молекулярная физика, 1990, §§13–14.
- Goussard, J.-O.; Roulet, B. (1993). "Free expansion for real gases". Am. J. Phys. 61: 845–848.
- Сивухин Д. В., Термодинамика и молекулярная физика, 1990, Уравнение (19.3), с. 71–72.
- Ландау Л. Д., Лифшиц Е. М. Статистическая физика. Часть 1, 2002, Уравнение (18.1).
- Сивухин Д. В., Термодинамика и молекулярная физика, 1990, Уравнение (46.1), с. 143.
- Ландау Л. Д., Лифшиц Е. М. Статистическая физика. Часть 1, 2002, Уравнение (18.2).
Литература
- Зубарев Д. Н. Джоуля — Томсона эффект // Физическая энциклопедия / Гл. ред. А. М. Прохоров. — М.: Советская энциклопедия, 1988. — Т. 1: Ааронова-Бома эффект — Длинные линии. — С. 605. — 704 с.
- Ландау Л. Д., Лифшиц Е. М. Статистическая физика. Часть 1. — Издание 5-е. — М.: Физматлит, 2002. — 616 с. — («Теоретическая физика», том V). — ISBN 5-9221-0054-8.
- Савельев И. В. Курс общей физики. — М.: КноРус, 2012. — Т. 1. Механика. Молекулярная физика и термодинамика. — 528 с. — ISBN 9785406025888.
- Сивухин Д. В. Общий курс физики. — Издание 3-е, исправленное и дополненное. — М.: Наука, 1990. — Т. II. Термодинамика и молекулярная физика. — 592 с. — ISBN 5-02-014187-9.
- Эффект Джоуля-Томсона В книге: В.М.Бродянский. От твердой воды до жидкого гелия (история холода). — М.: Энергоатомиздат, 1995.