Хэммонд, Джордж Симс
Джордж Симс Хэммонд (22 мая 1921, Оберн, штат Мэн, США — 5 октября 2005 Портленд, штат Орегон, США) — американский химик-теоретик, внёс большой вклад в развитие изучения фотохимии органических соединений [2], автор «Постулата Хэммонда» в теории переходного состояния в реакциях органической химии. Также известен своим вкладом в философию науки. [3] Лауреат Премии Норриса 1968, Медали Пристли 1976, Национальной научной медали США [4] , Золотой Медали Отмэра 2003 [5][6] . Был в должности председателя Allied Chemical Corporation с 1979 по 1989 год. Хэммонд получил степень бакалавра в Бэйтс-колледже в 1943 году, степень доктора наук в Гарвардском университете в 1947 году, работал в Оксфордском университете, в Базельском университете, в Национальном научном фонде США, в Калифорнийском технологическом институте, впоследствии возглавлял в нём одновременно химический факультет и факультет химической инженерии. С 1974 по 1978 он работал начальником отдела иностранных связей в национальной академии наук США.
| Джордж Симс Хэммонд | |
|---|---|
| George Simms Hammond | |
 <Джордж Симмс Хэммонд> | |
| Дата рождения | 22 мая 1922 |
| Место рождения | Оберн, Мэн, США |
| Дата смерти | 5 октября 2005[1] (84 года) |
| Место смерти | Портленд, Орегон, США |
| Страна | |
| Научная сфера | химия |
| Место работы | |
| Альма-матер | |
| Научный руководитель | Пол Даути Бартлетт |
| Награды и премии | |
Биография
Ранние годы и образование
Джордж Симонс Хэммонд родился 22 мая 1921 года в Оберне в штате Мэн [2]. Его семья работала на молочной ферме недалеко от дома, на улице Хардскрэппл. Его отец умер, когда Хэммонду было 13. Он был самым старшим из семерых детей, и их всех вырастила мать [2]. С раннего возраста Хэммонд работал на ферме с матерью, братьями и сестрами. До шестого класса он обучался на дому, а затем до выпуска в 1938 ходил в разные государственные школы Оберна. После выпуска он год не учился, работая на ферме. Затем он поступил в колледж Бейтс в Льюистоне. Выпустился оттуда magna cum laude, получив степень бакалавра наук по химии в 1943 году. Во время обучения состоял в обществе Phi Beta Kappa [2]. Начало карьеры Окончив колледж, Хэммонд пошел работать химиком в Rohm and Haas в Филадельфии, штат Пенсильвания. После нескольких месяцев работы он ушел продолжать учёбу в Гарвард. Он получил степень магистра и доктора философии. Его диссертация по теме «Ингибирование полимеризации аллилацетата» получила отзыв от Пола Бартлетта. Хэммонд переехал в Лос-Анджелес в Калифорнийский университет [2].
Работа в учебных заведениях
В 1948 Хэммонд начал преподавать в государственном колледже Айовы. Он работал ассистентом. Там он опубликовал постулат Хэммонда, который стал одним из самых важных текстов в области органической фотохимии. Он проводил исследования в Оксфордском и Базельском университетах по стипендии Гуггенхайма и по стипендии национального научного фонда соответственно. В 1958 он стал профессором органической химии в Калифорнийском технологическом институте [2]. Позже он был назначен профессором химии в лаборатории Артура Амоса Нойеса, а впоследствии стал руководить кафедрами химии и химической инженерии. Через 14 лет преподавания в Калифорнийском технологическом институте, в 1972 году он перевелся в университет Санта-Клары. В Санта Кларе он работал как профессором, так и деканом факультета естественных наук [7].
Дальнейшая карьера
В 1974 году был назначен «министром иностранных дел» в Национальной академии наук США, и проработал на этой должности один срок, уйдя в отставку в 1978. Хэммонд произносил несколько речей по важным политическим повесткам — например, по вторжению в Камбоджу, а также о важности интересовавших его химических исследований. Некоторые речи негативно отразились на его жизни, к примеру, Никсон вычеркнул его имя из списка руководителей Национальной академии наук [8]. В 1979 он ушел из преподавания и присоединился к Allied Corp. в качестве председателя. Там он работал 10 лет и ушел оттуда по окончании контракта [2].
Семейная жизнь
Хэммонд женился на Мариан Риз в 1945 году, имел от неё пятерых детей. Пара развелась в 1975 году, а он заново женился на Ив Менгер. С Ив у него было двое детей [2].
Постулат Хэммонда
Постулат Хэммонда (Основная статья)
В 1955 году Хэммонд опубликовал гипотезу о пространственном строении интермедиатов органических реакций. Первоначально гипотеза звучала следующим образом:
«Если две пространственные структуры, например, переходного состояния и нестабильного интермедиата, возникают последовательно в ходе химической реакции и имеют схожую свободную энергию, то их взаимопревращение требует малой реорганизации пространственной структуры.»[9]
В связи с этим геометрия переходного состояния может быть предсказана по энергии соседних соединений на координате реакции. Например, при экзотермической реакции переходное состояние ближе по энергии к реагентам, чем к продуктам. Поэтому геометрия переходного состояния будет напоминать реагент больше чем продукт. В процессе эндотермической реакции, напротив, переходное состояние схоже с продуктом. [10] Возможность подобного теоретического сравнения необычайна важна ввиду того, что промежуточные состояния превращающихся химических соединений редко могут быть экспериментально охарактеризованы ввиду нестабильности. [11] Постулат Хэммонда проясняет и рационализирует принцип Бэлла-Эванса-Поляни, который описывает эмпирическую зависимость скорости реакции, а значит и энергии активации процесса, от энтальпии процесса. Постулат Хэммонда объясняет эту зависимость, включая в описание закономерности в изменении геометрии переходного состояния, а также говорит о том, как в зависимости от изменения геометрии реагента, продукта, переходного состояния и интермедиата может меняться энергия активации реакции.[12] Постулат используется для предсказания зависимости энергии от координаты реакции. Например, ароматическое электрофильное замещение включает интермедиат и ещё два нестабильных переходных состояния. При изучении эффекта заместителей в этой реакции с применением постулата Хэммонда было установлено, что скорость-лимитирующая стадия заключается в перегруппировке интермедиата во второй переходное состояние перед появлением продукта.[13] В течение 1940-ых и 1950-ых годов, химики-органики искали причину возможных сильных изменений в скорости реакции и в составе продуктов реакции из-за небольших изменений в строении реагентов, и в 1955 году Джордж Хэммонд, молодой профессор Государственного университета Айовы постулировал, что теория переходного состояния может количественно описывать эти закономерности. Примечательно что в 1953 году похожая идея была предложена Джоном Леффлером из униерситета флориды [14]. Как бы то ни было, теория Хэммонда привлекла к себе больше внимания ввиду более доступного изложения и простого использования. Поэтому постулат Хэммонда иногда называют постулатом Хэммонда-Леффлера. [13]
Интерпретация постулата
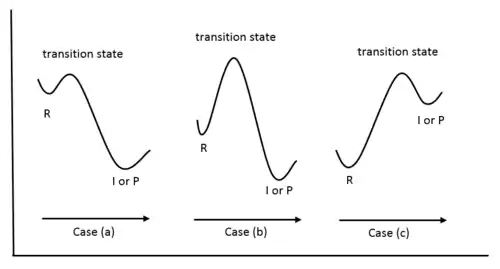
В целом, смысл постулата заключается в том, что структура переходного состояния ближе к структуре соединения, чья свободная энергия ближе к энергии переходного состояния. Это может быть проиллюстрировано с помощью зависимости свободной энергии реакции от координаты реакции. В случае (а) изображена экзотермическая реакция, здесь, очевидно, структура переходного состояния ближе к структуре реагента. На рисунке (b) изображена ситуация, когда свободная энергия переходного состояния не близка ни к продукту, ни к реагенту, в связи с чем можно сделать вывод, что структура переходного состояния не походит на структуру реагента или продукта. Случай (c) описывает эндотермическую реакцию, в которой, следуя постулату, переходное состояние ближе к интермедиату или к продукту. Важность постулата Хэммонда заключается в возможности обсуждать изменение геометрии химического соединения в процессе протекания химической реакции. Переходное состояние более близкое к реагенту называется «ранним», а более близкое к продукту или интермедиату «поздним» [15]. Примером «раннего» переходного состояния служит предполагаемое промежуточное соединение реакции хлорирования. Хлорирование является экзотермической реакцией, значит, свободная энергия продукта реакции ниже, чем реагента [16]. Поэтому переходное состояние по геометрии схоже с реагентом, возникает на координате реакции немного после начала превращения. Бромирование, напротив, эндотермическая реакция, значит, возникает «позднее» переходное состояние, близкое к окончанию реакции.[17] Ещё одной полезной интерпретацией постулата Хэммонда является возможность аппроксимировать совокупность структур нестабильных интермедиатов и переходных состояний рядом гипотетических интермедиатов.
Реакции SN1
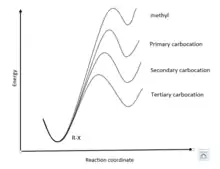
Постулат Хэммонда может быть использован для выяснения структуры переходного состояния реакции SN1. Диссоциация уходящей группы, первое переходное состояние реакции SN1, является скорость-лимитирующей стадией. Стабильность карбокатионов, образующихся в процессе диссоциации уменьшается в ряду четвертичный> третичный> вторичный> первичный, энергия активации реакции увеличивается в этом ряду, поэтому более стабильный и более близкий по величине свободной энергии к реагенту – четвертичный карбокатион. Первичный карбокатион, напротив, имея высокую величину свободной энергии, близкую по величине к энергии интермедиата.
Реакции SN2
В реакциях бимолекулярного нуклеофильного замещения скорость-лимитирующей стадией является образование переходного состояния из молекул реагентов. После образования переходного состояния реакция протекает стремительно. [18] В этом случае, напротив, чем менее стабильно переходное состояние, тем ближе оно к реагенту. [19]
Реакции Е1
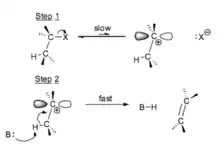
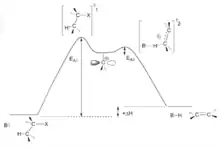
В реакциях Е1 скорость-лимитирующей стадией является отщепление уходящей группы, это двустадийный процесс. Более стабильный промежуточный карбокатион определяет продукт реакции. Стабилизация переходного состояния снижает энергию активации процесса. Способность к протеканию реакции уменьшается в ряду четвертичный> третичный> вторичный> первичный промежуточный карбокатион [20]. В процессе реакции образуется два независимых переходных энантиомерных состояния, превращающиеся в два различных продукта, и, согласно постулату Хэммонда, быстрее образуется тот продукт, которому отвечает переходное состояние с меньшей энергией активации. [21]
Реакции Е2
Скорость-лимитирующей стадией бимолекулярного элиминирования является образование переходного состояние из молекулы субстрата и основания. По этим соединениям наблюдается первый кинетический порядок реакции, скорость реакции зависит от стереохимии процесса, уходящей группы и силы основания. Существует отдельная теория для данного типа реакции, разработанная Джозефом Буннеттом, которая говорит об определяющей роли в высоте энергетического барьера углов Cβ-H и Cα-X в переходном состоянии. [22]
Связь принципа Бэлла-Эванса-Поляни (БЭП) с постулатом Хэммонда
Принцип БЭП гласит:
Для однотипных элементарных процессов имеется тесное соответствие между кинетическими и термодинамическими параметрами процесса, а именно существует линейная зависимость между тепловым эффектом H и энергией активации E процесса: E=a+bH, где a и b – линейные коэффициенты. [23]

Формально, постулат Хэммонда описывает только геометрию переходного состояния химической реакции. Как бы то ни было, постулат Хэммонда может дать информацию о скорости протекания реакции и энергии активации, а также даёт теоретическое объяснение принципа Бэлла-Эванса-Поляни, которое описывает связь теплового эффекта реакции с энергией активации. Связь этих двух концепций можно проиллюстрировать на примере реакций SN1. Диссоциация уходящей группы – скорость-лимитирующая стадия процесса, поэтому энергия активации всей реакции можно считать энергией активации только процесса диссоциации. Исходя из принципа БЭП, энергия активации реакции SN1 ниже в случае четвертичного переходного карбокатиона, что следует из меньшего отрицательного теплового эффекта (меньшей энтальпии). Вместе с тем, принцип БЭП не уточняет, почему наблюдаются эти эмпирические закономерности. Постулат Хэммонда устанавливает связь геометрии четвертичного переходного состояния с геометрией других соединений на координате реакции, глубже описывая данную эмпирическую зависимость.
Применение постулата
Постулат Хэммонда полезен для понимания взаимосвязи скорости реакции и стабильности продуктов. В то время как скорость реакции зависит только от энергии активации, равновесные концентрации продуктов зависят только от значений термодинамических потенциалов, то есть стабильности продуктов. Постулат Хэммонда связывает скорость процесса и структурные особенности состояний, возникающих по мере протекания процесса. В то время как очевидным является ожидание появления в продуктах реакции наиболее термодинамически стабильного соединения, важным фактором в появлении того или иного продукта является геометрия того или иного интермедиата.
Критика постулата
Постулат Хэммонда перестаёт описывать закономерности в появлении продуктов реакции в области высоких температур, где наблюдается не кинетический, но термодинамический контроль пути протекания реакции ввиду больших динамических возможностей (согласно статистической термодинамике) молекулы при высокой температуре.
Примечания
- George S. Hammond // Музей Соломона Гуггенхайма — 1937.
- Wamser, Carl C. Biography of George S. Hammond (англ.) // The Journal of Physical Chemistry A : journal. — 2003. — 1 May (vol. 107, no. 18). — P. 3149—3150. — ISSN 1089-5639. — doi:10.1021/jp030184e. — .
- Fox and Whiteshell, Marye Anne and James K. Organic Chemistry (неопр.). — Sudbury, Massachusetts: Jones and Bartlett Publishers, 2004. — С. 355—357. — ISBN 0-7637-2197-2.
- "Obituaries", C&EN, 83(48), 46 (November 28, 2005).
- Chemical Heritage Foundation names John Baldeschwieler and George Hammond 2003 Othmer Gold Medalists, Eureka Alert (1 апреля 2003). Дата обращения 12 июня 2014.
- Othmer Gold Medal. Science History Institute. Дата обращения: 22 марта 2018.
- Weiss, Richard G.; Wamser, Carl C. Introduction to the Special Issue in honour of George Simms Hammond (англ.) // Photochemical & Photobiological Sciences : journal. — The Royal Society of Chemistry and Owner Societies, 2006. — Vol. 5, no. 10. — P. 869—870. — doi:10.1039/b612175f.
- Wamser, Carl C. Biography of George S. Hammond (англ.) // The Journal of Physical Chemistry A : journal. — 2003. — May (vol. 107, no. 18). — P. 3149—3150. — ISSN 1089-5639. — doi:10.1021/jp030184e.
- Hammond, G. S. A Correlation of Reaction Rates (англ.) // J. Am. Chem. Soc. : journal. — 1955. — Vol. 77. — P. 334—338. — doi:10.1021/ja01607a027. Solomons, T.W. Graham & Fryhle, Craig B. (2004). Organic Chemistry (8th ed.). John Wiley & Sons, Inc. ISBN 0-471-41799-8.
Loudon, G. Marc. "Organic Chemistry" 4th ed. 2005. - Carey, Francis A.; Sundberg, Richard. Advanced Organic Chemistry Part A:Structure and Mechanisms (англ.). — Norwell: Springer, 2007.
- Anslyn, Eric V.; Dougherty, Dennis A. Modern Physical Organic Chemistry (неопр.). — Sausalito, CA: University Science, 2006.
- McMurry, John. Organic Chemistry (неопр.). — Pacific Grove, CA: Brooks/Cole, 1992. — С. 246—248.
- Carey, F.A.; Sundberg, R.J. Advanced Organic Chemistry.-Part A: Structure and Mechanism (англ.). — New York, NY: Plenum, 1990.
- Leffler, J. E. Parameters for the Description of Transition States (англ.) // Science : journal. — 1953. — Vol. 117. — P. 340—341. — doi:10.1126/science.117.3039.340. — .
- Meany, J.E. Application of Hammond's postulate (англ.) // Journal of Chemical Education : journal. — 2001. — 1 February (vol. 01, no. 78). — P. 204. — doi:10.1021/ed078p204. — .
- Fox, Marye Anne; Whitesell, James K. Organic Chemistry Third Edition (неопр.). — Sudbury, MA: Jones and Barlett Publishers, 2004. — С. 356.
- Sorrell, Thomas N. Organic Chemistry Third Edition (неопр.). — Sausalito, CA: University Science Books, 2005. — С. 370—371.
- Anslyn, Eric V.; Brown, William H.; Foote, Christopher S.; Iverson, Brent L. Organic Chemistry Fifth Edition (неопр.). — Belmont, CA: Brooks/Cole Cengage Learning, 2009. — С. 333.
- Curtis, Rachael Kinetics of Nucleophilic Substitution Reactions. Chemwiki. UCDavis (2 октября 2013). Дата обращения: 21 ноября 2015.
- Justik, Michael W. Review of SN1, SN2, E1, and E2.
- Rajendran, Kamalraj V.; Nikitin, Kirill V.; Gilheany, Declan G. Hammond Postulate Mirroring Enables Enantiomeric Enrichment of Phosphorus Compounds via Two Thermodynamically Interconnected Sequential Stereoselective Processes (англ.) // Journal of the American Chemical Society : journal. — 2015. — 17 July (vol. 137, no. 29). — P. 9375—9381. — doi:10.1021/jacs.5b04415. — PMID 26186272.
- Bunnett, Joseph. Survey of Progress in Chemistry (неопр.). — New York: Academic, 1962. — С. 70—72.
- Ориентация — Студопедия