Постулат Хэммонда
Постулат Хэммонда (принцип Хэммонда) — гипотеза в области физической органической химии, предложенная американским химиком Джорджем Хэммондом. Эта гипотеза гласит, что если переходное состояние ведёт к неустойчивому интермедиату (или продукту), то оно имеет приблизительно такую же энергию, как этот интермедиат (продукт). Переход между этими двумя состояниями осуществляется за счёт лишь малого изменения структуры молекулы[1].
Напротив, если рассматриваемая стадия процесса ведёт к продукту, более устойчивому, чем субстрат, то переходное состояние структурно и энергетически близко к неустойчивому субстрату. Соответственно, постулат Хэммонда иногда формулируют следующим образом:
Структура переходного состояния может быть близкой как к продукту, так и к исходному веществу, в зависимости от того, к чему оно ближе по энергии. В экзотермических реакциях переходное состояние напоминает исходное вещество, а в эндотермических — продукт[2].
Постулат Хэммонда широко применяется в органической химии как инструмент для получения информации о переходном состоянии реакции, поскольку получить прямых экспериментальных данных о нём невозможно из-за слишком малого времени существования. Постулат же позволяет рассуждать о переходных состояниях, используя информацию о интермедиатах, реагентах и продуктах[3].
Графическая интерпретация
Постулат Хэммонда может быть легко объяснён на основании диаграмм потенциальной энергии для общих случаев экзотермической и эндотермической реакций.
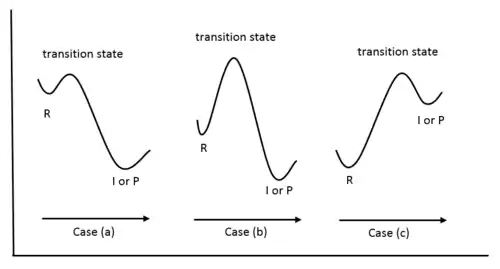
На рисунке (а) приведена диаграмма потенциальной энергии для экзотермической реакции, где продукт является более устойчивым, нежели исходное соединение. В этом случае переходное состояние, располагающееся в максимуме потенциальной энергии, близко по энергии к исходному соединению и структурно напоминает его. Такое переходное состояние называют ранним. Случай (с) изображает противоположную ситуацию: данная кривая характерная для потенциальной энергии эндотермической реакции. Продукт является более неустойчивым, поэтому переходное состояние близко и по энергии, и по структуре именно к нему, а не к исходному соединению. В данном случае его называют поздним. Случай (b) является промежуточным: реакция не обладает достаточно выраженным тепловым эффектом, чтобы можно было точно сказать, к продукту или исходному соединению ближе переходное состояние. Поэтому ни одно, ни другое не могут точно описать строение переходного состояния, и необходимо искать другую модель, применимую для данного случая[3].
Примеры использования в органической химии
Типичным примером использования постулата Хэммонда является обсуждение механизма реакций мономолекулярного нуклеофильного замещения. Первой и лимитирующей стадией таких процессов является диссоциация связи C–галоген и образование карбокатиона.
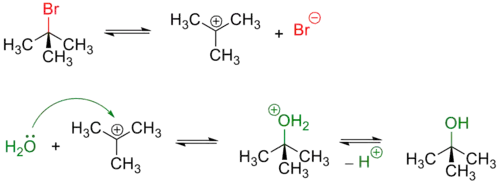
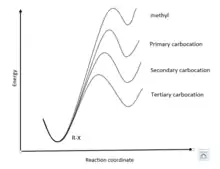
На этой стадии интермедиат (карбокатион) является более неустойчивым, чем исходный галогенид, поэтому переходное состояние является поздним и по структуре напоминает этот карбокатион. Если сравнивать устойчивость карбокатионов, образующихся из метилгалогенидов, первичных, вторичных и третичных галогенидов, то в этом ряду устойчивость будет повышаться, а их энергия понижаться. Но поскольку переходные состояния напоминают по структуре карбокатионы, то их энергия будет близка к энергии соответствующих карбокатионов и будет изменяться с той же тенденцией. Таким образом, постулат Хэммонда позволяет получать информацию о переходных состояниях, не имея реальных данных об их строении[4].
Примечания
- IUPAC Gold Book — Hammond principle (Hammond postulate). Дата обращения: 5 декабря 2014.
- H. J. Reich. Named Rules and Effects in Organic Chemistry. Дата обращения: 5 декабря 2014.
- Carey F. A., Sundberg R. J. Advanced Organic Chemistry: Part A: Structure and Mechanisms. — 5th Ed.. — Springer, 2007. — С. 289—290. — ISBN 978-0-387-44897-8.
- Anslyn E. V., Dougherty D. A. Modern Physical Organic Chemistry. — University Science Books, 2006. — С. 377.