Скорлупа
Скорлупа или путáмен (от лат. putamen — скорлупа) — базальное ядро, входит в состав стриопаллидарной системы и находится в основании переднего мозга (конечный мозг). Скорлупа, вместе с бледным шаром, образуют чечевицеобразное ядро, которое, в свою очередь, вместе хвостатым ядром образуют полосатое тело. С помощью различных путей скорлупа подключена к чёрной субстанции и бледному шару. Основными функциями скорлупы являются регулирование движения и влияние на различные виды обучения. В качестве главного нейротрансмиттера путамен использует дофамин. Путамен также играет роль в этиологии дегенеративных неврологических расстройств, таких как болезнь Паркинсона.
| Скорлупа | |
|---|---|
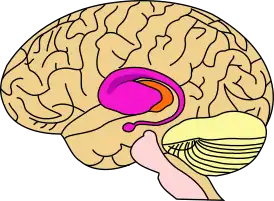 фиолетовый цвет = скорлупа, хвостатое ядро, миндалина, оранжевый = таламус | |
| Система | Стриопаллидарная |
| Каталоги | |
Происхождение названия
Происходит от латинского слова putáre, что означает думать или рассмотреть[2].
Анатомия

Скорлупа является базальным ганглием, расположенным в переднем мозге. Неразрывно связана с хвостатым ядром и бледным шаром, образуя полосатое тело и чечевицеобразное ядро. Является наиболее латеральной часть чечевицеобразного ядра.
Хвостатое ядро и скорлупа содержат те же типы нейронов и циклы — многими нейроанатомами рассматриваются как дорсальная часть стриатума, образуя единую структуру, разделённую на две части массивным пучком волокон, внутренней капсулой, проходящей между хвостатым ядром и скорлупой. Путамен вместе с бледным шаром составляют линзовидное ядро. Путамен является самой внешней частью базальных ганглиев. Это группы ядер в мозге, которые связаны между собой, с корой головного мозга, таламусом и стволом мозга.
Скорлупа взаимосвязана со следующими структурами:
- Хвостатое ядро
- Чёрная субстанция
- Бледный шар
Физиология
Для того чтобы контролировать движения, скорлупа должна взаимодействовать с другими структурами, которые составляют базальные ганглии. Они включают в себя — хвостатое ядро и бледный шар. Эти две структуры, наряду с скорлупой, взаимодействуют через ряд прямых и косвенных ингибирующих путей. Прямой путь состоит из двух ингибирующих путей от скорлупы к чёрной субстанции и внутренней области бледного шара. Этот путь в качестве нейротрансмиттеров использует — дофамин, ГАМК и вещество P. Косвенные пути состоят из трех ингибирующих путей, которые идут от скорлупы и хвостатого ядра к внешней области бледного шара. Но в отличие от прямого пути в данном пути используются в качестве нейротрансмиттеров дофамин, ГАМК и энкефалины. При взаимодействии прямого и косвенного путей происходят непроизвольные движения.
Дофамин
Дофамин является одним из главных нейромедиаторов, который регулируется путаменом.
Другие нейромедиаторы
Путамен также играет важную роль в модуляции других нейротрансмиттеров. Скорлупа вырабатывает ГАМК, энкефалины, вещество Р, и ацетилхолин. В качестве получаемых нейромедиаторов используется — серотонин и глутамат. Большинство из этих нейромедиаторов играют роль в управлении и координации движений[3].
Роль в обучении
Проведено множество исследований скорлупы, из которых стало очевидно, что она играет важную роль во многих типах обучения. Некоторые примеры приведены ниже:
Обучение с подкреплением и имплицитное обучение
Наряду с различными видами обучения, путамен также оказывает влияние на имлицитное и обучение с подкреплением[4].
Имплицитное обучение — является пассивным процессом, в котором люди подвергаются воздействию информации и приобретают знания с помощью экспозиции (различных внешних воздействий).
Управление моторикой
Путамен выполняет много функций, однако был сделан вывод, что она не имеет конкретной специализации. Но, так как скорлупа взаимосвязана со многими другими структурами, она работает в сочетании с ними, чтобы управлять многими типами моторных навыков. К ним относятся:
- управление обучения движений
- двигательная активность и задачи[5]
- подготовка движения[6]
- задача амплитуды движения[7]
- последовательность выполняемых движений[8].
Некоторые неврологи предполагают, что скорлупа также играет роль в выборе движения (например, при синдроме Туретта) и «автоматически» выполняет ранее изученное движение (например, при болезни Паркинсона)[9].
Роль в «цикле ненависти»
Последние, предварительные исследования показали, что путамен может выполнять функцию в так называемом «цикле ненависти» головного мозга. Недавнее исследование было сделано отделом клеточной и эволюционной биологии в Университетском колледже Лондона. В эксперименте была задействована группа добровольцев, у которых провели магнитно-резонансную томографию, пока они просматривали портреты людей — ненавистных для них персон, а также фотографии трех человек того же пола, к которым они относились нейтрально. В ходе эксперимента, «оценка ненависти» была записана для каждого снимка. Была также создана так называемая «шкала ненависти», включающая значения от 0 до 72 баллов. Результатом эксперимента послужила активация путамена, инсулы, медиальной фронтальной извилины и некоторых участков коры головного мозга (премоторная кора и фронтополярная кора). Ученым также удалось обнаружить связь между уровнем мозговой активности и оценкой, которую тестируемые присваивали фотографиям по вышеупомянутой 72-балльной шкале. Чем сильнее была ненависть, тем больше активизировались структуры мозга[10].
Патофизиология
Путамен играет важную роль в этиологии многих дегенеративных неврологических заболеваниях и расстройств.
Болезнь Паркинсона
После обнаружения у скорлупы основных функций стало очевидным, что она и базальные ганглии играют важную роль в этиологии болезни Паркинсона, а также других заболеваний, которые связаны с дегенерацией нейронов[11].
Болезнь Паркинсона является медленной, прогрессирующей и c устойчивой потерей дофаминергических нейронов в pars compacta чёрной субстанции. В развитии болезни Паркинсона путамен играет ключевую роль, потому что её входы и выходы непосредственно связаны с чёрной субстанцией и бледным шаром. При болезни Паркинсона деятельность в прямом пути к внутренней части бледного шара уменьшается, а активность в косвенных путях к внешней части бледного шара увеличивается. Вместе эти действия вызывают чрезмерное торможение таламуса. Именно поэтому пациенты-паркинсонисты страдают тремором и проблемами выполнения произвольных движений.
Другие заболевания и расстройства
Болезни и расстройства связаны с нарушениями путамена:
- Снижение когнитивных функций при болезни Альцгеймера[12]
- Болезнь Хантингтона
- Болезнь Вильсона-Коновалова
- Деменция с тельцами Леви
- Кортикобазальная дегенерация
- Синдром Туретта
- Шизофрения
- Депрессия
- Синдром дефицита внимания и гиперактивности[13]
- Хорея
- Обсессивно-компульсивное расстройство[14][15]
- Другие психические расстройства[15].
Примечания
- Putamen // Foundational Model of Anatomy
- Latin Definitions for: putare (Latin Search) — Latin Dictionary and Grammar Resources — Latdict
- Crutcher, Michael D. Telephone Interview. 19 November 2008.
- Packard MG; Knowlton B. J. Learning and memory functions of the Basal Ganglia (неопр.) // Annu Rev Neurosci.. — 2002. — Т. 25, № 1. — С. 563—593. — doi:10.1146/annurev.neuro.25.112701.142937. — PMID 12052921.
- DeLong MR; Alexander GE, Georgopoulos AP, Crutcher MD, Mitchell SJ, Richardson RT (1984). «Role of basal ganglia in limb movements». Human Neurobiology 2 (4): 235-44. PMID 6715208.
- Alexander GE; Crutcher MD (July 1990). «Preparation for movement: neural representations of intended direction in three motor areas of the monkey». Journal of Neurophysiology 64 (1): 133-50. PMID 2388061.
- Delong MR; Georgopoulos AP, Crutcher MD, Mitchell SJ, Richardson RT, Alexander GE (1984). «Functional organization of the basal ganglia: contributions of single-cell recording studies». Ciba Found Symp. 107: 64-82. PMID 6389041.
- Marchand WR; Lee JN, Thatcher JW, Hsu EW, Rashkin E, Suchy Y, Chelune G, Starr J, Barbera SS (June 11 2008). «Putamen coactivation during motor task execution». Neuroreport. 19 (9): 957—960. doi:10.1097/WNR.0b013e328302c873. PMID 18521000.
- Griffiths PD; Perry RH, Crossman AR (March 14 1994). «A detailed anatomical analysis of neurotransmitter receptors in the putamen and caudate in Parkinson’s disease and Alzheimer’s disease». Neuroscience Letters 169 (1-2): 68-72. doi:10.1016/0304-3940(94)90358-1. PMID 8047295.
- Британские нейрофизиологи выяснили, что ненависть активизирует мозг почти так же, как и любовь. Дата обращения: 9 апреля 2013. Архивировано 9 апреля 2013 года.
- DeLong MR; Wichmann T (January 2007). «Circuits and circuit disorders of the basal ganglia». Arch Neurol. 64 (1): 20-4. doi:10.1001/archneur.64.1.20. PMID 17210805.
- de Jong LW; van der Hiele K; Veer IM; Houwing JJ; Westendorp RG; Bollen EL; de Bruin PW; Middelkoop HA; van Buchem MA; van der Grond J. Strongly reduced volumes of putamen and thalamus in Alzheimer's disease: an MRI study. (англ.) // Brain : journal. — Oxford University Press, 2008. — December (vol. 131, no. 12). — P. 3277—3285. — doi:10.1093/brain/awn278. — PMID 19022861.
- Martin H. Teicher; Carl M. Anderson; Ann Polcari; Carol A. Glod; Luis C. Maas; Perry F. Renshaw. Functional deficits in basal ganglia of children with attention-deficit/hyperactivity disorder shown with functional magnetic resonance imaging relaxometry (англ.) // Nature Medicine : journal. — 2000. — Vol. 6, no. 12. — P. 470—473. — doi:10.1038/74737. — PMID 10742158.
- Radua, Joaquim; Mataix-Cols, David. Voxel-wise meta-analysis of grey matter changes in obsessive–compulsive disorder (англ.) // British Journal of Psychiatry : journal. — Royal College of Psychiatrists, 2009. — November (vol. 195, no. 5). — P. 393—402. — doi:10.1192/bjp.bp.108.055046. — PMID 19880927.
- Radua, Joaquim; van den Heuvel, Odile A.; Surguladze, Simon; Mataix-Cols, David. Meta-analytical comparison of voxel-based morphometry studies in obsessive-compulsive disorder vs other anxiety disorders (англ.) // Archives of General Psychiatry : journal. — 2010. — 5 July (vol. 67, no. 7). — P. 701—711. — doi:10.1001/archgenpsychiatry.2010.70. — PMID 20603451.
Литература
- Синельников Р. Д., Синельников Я. Р. Атлас анатомии человека в 4 томах. Т.3. — М.: Медицина, 1996. — ISBN 5-225-02723-7