Реакция Гаттермана
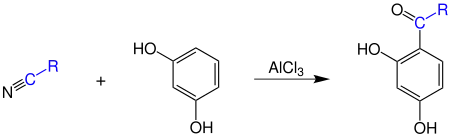
Реа́кция Га́ттермана — формилирование фенолов или их эфиров действием синильной кислоты и хлороводорода в присутствии кислот Льюиса (хлорид алюминия, хлорид меди (I), хлорид цинка и т. д.) в качестве катализаторов.
Данная реакция была открыта немецким химиком-органиком Людвигом Гаттерманом в 1898 году.
Механизм реакции
Реакция идет по механизму электрофильного замещения в ароматическом ряду SEAr.
На первом этапе происходит присоединение хлороводорода к аддукту синильной кислоты и кислоты Льюиса (хлорида цинка) с образованием комплекса формимидхлорида 1. При избытке хлорида цинка комплекс формимидхлорида образует карбениевый ион, выступающий в роли электрофила и присоединяющийся к ароматическому соединению с образованием σ-комплекса 2, который реароматизируется с отщеплением протона и образованием иминиевой соли 3.
Гидролиз иминиевой соли через образование аминоспирта 4 и отщепление иона аммония ведет к альдегиду 5:

Применимость и модификации
Реакция используется, в первую очередь, для формилирования эфиров фенолов, формилирование идет в пара-положение по отношению к OR, а если это место занято, то в орто-положение. Реакцию проводят в эфире, хлорбензоле, о-дихлорбензоле , тетрахлорэтилене, выходы до 80%. В реакцию также вступают электронобогащенные гетероциклические соединения - пирролы, фураны, тиофены.
Во избежание применения ядовитой синильной кислоты, Роджер Адамс в 1923 году модифицировал условия реакции, заменив циановодород цианидом цинка. Это позволило из цианида цинка и HCl получать непосредственно в реакционной смеси HCN и безводный хлорид цинка, играющий роль слабой кислоты Льюиса (а значит, и катализатора реакции). Используя эту модификацию, можно получать выход альдегидов из фенолов и их эфиров более 90 %, и повысить выход реакций с ароматическими углеводородами.
Модификация английского химика Леонарда Хинкеля (1882—1962) (была открыта в 1936 г.) предусматривает использование в качестве катализатора AlCl3 • 2HCl в хлорбензоле и 1,2-дихлорэтане, что позволяет формилировать многоядерные ароматические углеводороды, в частности, фенантрен.
Кроме того, вместо цианидов для введения формильной группы можно использовать нетоксичный и легко доступный симметричный 1,3,5-триазин. Этот метод обеспечивает высокие выходы альдегидов при формилировании алкилбензолов, фенолов, эфиров фенолов, конденсированных углеводородов и гетероциклических соединений.
Родственные раекции
В качестве электрофильного компонента вместо синильной кислоты могут быть использованы нитрилы, конечным продуктом в этом случае являются ароматические кетоны (реакция Губена — Геша):
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1 (Абл-Дар). — 623 с.