Эмбелин
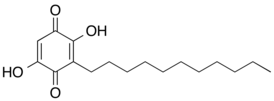
Эмбелин (2,5-дигидрокси-3-ундецил-1,4-бензохинон) представляет собой встречающийся в природе парабензохинон, выделенный из сушеных ягод растений Embelia ribes из подсемейства Мирсиновые, часто называемых "фальшивым черным перцем".[1][2][3]
| Эмбелин | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
2,5-дигидрокси-3-ундецилциклогекса-2,5-диен-1,4-дион |
| Хим. формула | C17H26O4 |
| Физические свойства | |
| Состояние | порошок |
| Молярная масса | 294.183 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 142-143 ºC |
| Химические свойства | |
| Растворимость | |
| • в воде | практически не растворим |
| Классификация | |
| Рег. номер CAS | 550-24-3 |
| PubChem | 3218 |
| Рег. номер EINECS | 208-979-8 |
| SMILES | |
| InChI | |
| ChEBI | 4778 |
| ChemSpider | 3105 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Эмбелин и его производные обладают широким спектром биологической активности[4][5], включая антиоксидантную[6], противоопухолевую[7][8], противовоспалительную и анальгезирующую[9], противомикробную[10], антидиабетическую[11][12], анксиолитическую[13], а также противозачаточную.[14][15] и антисперматогенную.[16]
Лечение эмбелином значительно снижает вызванное паракватом повреждение легких за счет подавления окислительного стресса, воспалительного каскада (высвобождение воспалительных цитокинов) и сигнального пути MAPK/NF-κB у крыс, отравленных паракватом.[17]. Эмбелин и его производные, такие как RF22-c избирательно ингибируют 5-LOX и микросомальную простагландин Е2-синтазу-1[18] [19][20]
Примечания
- Radhakrishnan, N., & Gnanamani, A. (2014). 2, 5-dihydroxy-3-undecyl-1, 4-benzoquinone (Embelin)-A second solid gold of India-A Review. International Journal Pharmacy & Pharmaceutical Sciences, 6(6), 23-30.
- Poojari, R. (2014). Embelin–a drug of antiquity: shifting the paradigm towards modern medicine. Expert opinion on investigational drugs, 23(3), 427-444. PMID 24397264 doi:10.1517/13543784.2014.867016
- Kamble, V., Attar, U., Umdale, S., Nimbalkar, M., Ghane, S., & Gaikwad, N. (2020). Phytochemical analysis, antioxidant activities and optimized extraction of embelin from different genotypes of Embelia ribes Burm f.: a woody medicinal climber from Western Ghats of India. Physiology and Molecular Biology of Plants, 26(9), 1855-1865. PMID 32943821 PMC 7468010 doi:10.1007/s12298-020-00859-2
- Othman, S. N. N., Lum, P. T., Sekar, M., Mazlan, N. A., Yusri, P. Z. S., Ghazali, N. F., ... & Noor, A. A. M. (2020). Molecules of Interest–Embelin–A Review. Research Journal of Pharmacy and Technology, 13(7), 3485-3493. doi:10.5958/0974-360X.2020.00618.6
- Souravi, K., & Rajasekharan, P. E. (2014). Ethnopharmacological Uses of Embelia ribes Burm. F. A Review. IOSR Journal of Pharmacy and Biological Sciences, 9(3), 23-30. doi:10.9790/3008-09332330
- Joshi R, Kamat JP, Mukherjee T. (2007). Free radical scavenging reactions and antioxidant activity of embelin: biochemical and pulse radiolytic studies. Chem-Biol Interact;167:125–134. PMID 29620447 doi:10.4155/fmc-2017-0198
- Prabhu KS, Achkar IW, Kuttikrishnan S, et al. (2018). Embelin: a benzoquinone possesses therapeutic potential for the treatment of human cancer. Future Med Chem;10:961–976. PMID 29620447 doi:10.4155/fmc-2017-0198
- Ko JH, Lee SG, Yang W, et al. (2018). The application of embelin for cancer prevention and therapy. Molecules;23:621. PMID 29522451 PMC 6017120 doi:10.3390/molecules23030621
- Mahendran S, Badami S, Ravi S, et al. (2011). Synthesis and evaluation of analgesic and anti-inflammatory activities of most active free radical scavenging derivatives of embelin – a structure-activity relationship. Chem Pharm Bull;59:913–9. PMID 21804233 doi:10.1248/cpb.59.913
- Chitra M, Shyamala Devi CS, Sukumar E. (2003). Antibacterial activity of embelin. Fitoterapia;74:401–403. PMID 12781816 doi:10.1016/s0367-326x(03)00066-2
- Durg, S., Veerapur, V. P., Neelima, S., & Dhadde, S. B. (2017). Antidiabetic activity of Embelia ribes, embelin and its derivatives: A systematic review and meta-analysis. Biomedicine & Pharmacotherapy, 86, 195-204. PMID 27984799 doi:10.1016/j.biopha.2016.12.001
- Chen, X., Gao, M., Jian, R., Hong, W. D., Tang, X., Li, Y., ... & Wu, P. (2020). Design, synthesis and α-glucosidase inhibition study of novel embelin derivatives. Journal of Enzyme Inhibition and Medicinal Chemistry, 35(1), 565-573. PMID 31969031 PMC 7006637 doi:10.1080/14756366.2020.1715386
- Afzal M, Gupta G, Kazmi I, et al. (2012). Evaluation of anxiolytic activity of embelin isolated from Embelia ribes. Biomed Aging Pathol;2:45–7. doi:10.1016/j.biomag.2012.03.003
- Agrawal, S., Chauhan, S., & Mathur, R. (1986). Antifertility effects of embelin in male rats. Andrologia, 18(2), 125-131. PMID 3717601 doi:10.1111/j.1439-0272.1986.tb01749.x
- Wango, E. O. (2005). Anti-fertility effects of embelin in female Sprague-Dawley rats may be due to suppression of ovarian function. Acta Biologica Hungarica, 56(1-2), 1-9. PMID 15813209 doi:10.1556/ABiol.56.2005.1-2.1
- Gupta, S., Sanyal, S. N., & Kanwar, U. (1989). Antispermatogenic effect of embelin, a plant benzoquinone, on male albino rats in vivo and in vitro. Contraception, 39(3), 307-320. PMID 2714091 doi:10.1016/0010-7824(89)90063-2
- SreeHarsha, N. (2020). Embelin impact on paraquat‐induced lung injury through suppressing oxidative stress, inflammatory cascade, and MAPK/NF‐κB signaling pathway. Journal of Biochemical and Molecular Toxicology. PMID 32020686 doi:10.1002/jbt.22456
- Schaible, A. M., Traber, H., Temml, V., Noha, S. M., Filosa, R., Peduto, A., Weinigel, C., Barz, D., Schuster, D., Werz, O. (2013). Potent inhibition of human 5-lipoxygenase and microsomal prostaglandin E2 synthase-1 by the anti-carcinogenic and anti-inflammatory agent embelin. Biochemical pharmacology, 86(4), 476-486. PMID 23623753 doi:10.1016/j.bcp.2013.04.015
- Filosa, R., Peduto, A., Schaible, A. M., Krauth, V., Weinigel, C., Barz, D., ... & D'Agostino, B. (2015). Novel series of benzoquinones with high potency against 5-lipoxygenase in human polymorphonuclear leukocytes. European Journal of Medicinal Chemistry, 94, 132-139. PMID 25765759 doi:10.1016/j.ejmech.2015.02.042
- Liparulo, A., Esposito, R., Santonocito, D., Muñoz-Ramírez, A., Spaziano, G., Bruno, F., ... & D'Agostino, B. (2020). Formulation and Characterization of Solid Lipid Nanoparticles Loading RF22-c, a Potent and Selective 5-LO Inhibitor, in a Monocrotaline-Induced Model of Pulmonary Hypertension. Frontiers in Pharmacology, 11, 83. PMID 32180715 PMC 7059131 doi:10.3389/fphar.2020.00083