Полиаминокарбоновые кислоты
Полиаминокарбоновые кислоты (комплексоны) — молекулы, в которых с атомом азота связано несколько алкилкарбоксильных групп —СН2СООН, способных одновременно связывать центральный атом комплекса несколькими координационными связями. Комплексоны образуют прочные, растворимые в воде соединения с большинством катионов.
Примеры
Наиболее простым представителем комплексонов является аминокислота глицин, H2NCH2COOH. В молекуле глицина аминогруппа NH2 отделена от карбоксильной группы COOH единственной метиленовой группой CH2. Когда карбоксильная группа депротонирована, ион глицина может являться бидентатным лигандом и образовывать хелатные комплексы с ионами металлов[1].
Другие примеры комплексонов[2]:
- Тридентатные - иминодиуксусная кислота
- Тетрадентатные - нитрилуксусная, нитрилтриметиленфосфоновая кислоты
- Пентадентатные - N-этилэтилендиамин-N,N',N'-триуксусная кислота
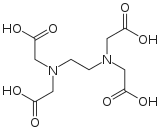
- Гексадентатные - этилендиаминтетрауксусная, о-фенилендиаминтетрауксусная, о-фенилендиамин-N,N-бис(диметиленфосфоновая) кислоты
- Гептадентатные - 2-гидрокси-1,3-диаминопропилен-N,N,N',N'-тетрауксусная кислота
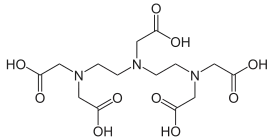
- Октадентатные - диэтилентриаминпентауксусная кислота
 |
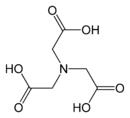 | |
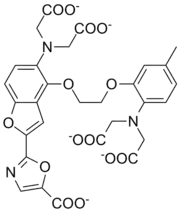
| Fura-2 | иминодиуксусная кислота[3] | нитрилотриуксусная кислота[4] |
 |
 |
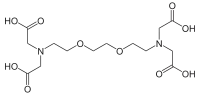 |
| EDTA | DTPA[3] | EGTA |
Примечания
- Schwarzenbach, G. Der Chelateffekt (англ.) // Helv. Chim. Acta : journal. — 1952. — Vol. 35. — P. 2344—2359. — doi:10.1002/hlca.19520350721.
- Основы аналитической химии, 2004.
- Anderegg, G.; Arnaud-Neu, F.; Delgado, R.; Felcman, J.; Popov, K. Critical evaluation of stability constants of metal complexes of complexones for biomedical and environmental applications* (IUPAC Technical Report) (англ.) // Pure Appl. Chem., : journal. — 2005. — Vol. 77, no. 8. — P. 1445—1495. — doi:10.1351/pac200577081445. pdf
- Anderegg, G. Critical survey of stability constants of NTA complexes (англ.) // Pure Appl. Chem., : journal. — 1982. — Vol. 54, no. 12. — P. 2693—2758. — doi:10.1351/pac198254122693. pdf
Литература
- Основы аналитической химии / под ред. Ю. А. Золотова. — 3-е , перераб. и доп. — М.: Высш. шк., 2004. — Т. 2. — 503 с. — (Классический университетский учебник).
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.