Налмефен
Налмефен (торговые наименования «Селинкро», «Revex») — антагонист опиоидных рецепторов с преимущественным сродством к κ-опиоидным рецепторам и, в несколько меньшей степени, к μ-опиоидным рецепторам, разработанный в начале 1970-х гг.[1].
| Налмефен | |
|---|---|
 | |
| Химическое соединение | |
| ИЮПАК | 17-cyclopropylmethyl-4,5α-epoxy-6-methylenemorphinan-3,14-diol |
| Брутто-формула | C21H25NO3 |
| Молярная масса | 339.43 г/моль |
| CAS | 55096-26-9 |
| PubChem | 5284594 |
| DrugBank | 06230 |
| Состав | |
| Классификация | |
| АТХ | N07BB05 |
| Фармакокинетика | |
| Связывание с белками плазмы | 45% |
| Метаболизм | hepatic |
| Период полувывед. | 10.8 ± 5.2 hours |
| Экскреция | renal |
| Способы введения | |
| Oral, Intravenous | |
В 1995 году налмефен в виде раствора для инъекций (0,1 и 1 мг/мл) был одобрен FDA под торговым наименованием «Revex» в качестве антидота опиоидных агонистов, в том числе для лечения передозировки наркотических анальгетиков[2]. В настоящее время «Revex» снят с производства[3].
В 2013 году налмефен в виде таблеток (18 мг) был одобрен EMA под торговым наименованием «Selincro» для лечения алкогольной зависимости. C 2015 г. доступен и на рынке Российской Федерации под торговым наименованием «Селинкро».
Налмефен — первое и, пока, единственное зарегистрированное лекарственное средство, предназначенное для сокращения потребления алкоголя, а не полного воздержания от него.
В результате применения налмефена пациентами с алкогольной зависимостью, расходы здравоохранения на лечение и профилактику пагубных последствий употребления алкоголя снижаются уже через год[4].
Фармакология
Фармакодинамика
Налмефен — опиоидный антагонист с преимущественным сродством к κ-опиоидному (KOP) и μ-опиоиднму (MOP) рецептору. Сродство (аффинность, Ki) к KOP рецептору в 3 раза выше, чем к MOP и составляет 0.08 нМ и 0.24 нМ, соответственно[5].
К δ-опиоидному (DOP) рецептору налмефен проявляет сравнительно низкое сродство (16 нМ)[5].
Налмефен является частичным (парциальным) агонистом κ-опиоидного рецептора с низкойвнутренней активностью (эффективностью агонизма, Emax=29 %)[5].
Налмефен является нейтральным антагонистом μ-опиоидного рецептора[5].
Эндогенная опиоидная система является одним из главных модуляторов функциональной активности мезокортикальных и мезолимбических дофаминергических нейронов, вовлеченных в процесс формирования положительного и отрицательного подкрепления. Доклинические данные свидетельствуют о том, что, проявляя свойства частичного агониста KOP, налмефен может выступать в роли их функционального антагониста в условиях, связанных с избыточностью нейротрансмиссии, опосредованной динорфином, и, таким образом, может уменьшать отрицательные подкрепляющие эффекты алкоголя в виде аверсивных состояний, возникающих при прекращении его приема. Проявляя свойства антагониста MOP, налмефен может снижать опосредованное β-эндорфином положительное подкрепляющее действие алкоголя.
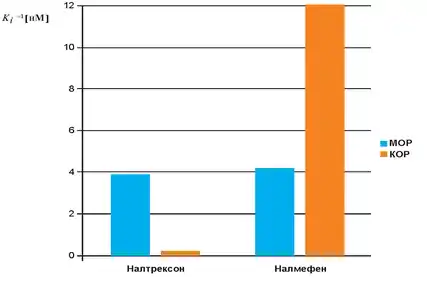
Различие профилей рецепторного связывания налмефена и налтрексона
Налмефен отличается от налтрексона замещением кетоновой группы (=О, в положении 6) на метиленовую (=CH2), что кардинально (в 64 раза) увеличивает аффинность к κ-опиоидному рецептору:
| Аффинность (Ki, нМ) налмефена и налтрексона к трём классическим типам опиоидных рецепторов | |||
|---|---|---|---|
| Соединение | MOP (μ) | KOP (κ) | DOP (δ) |
| Налмефен[5] | 0,24 | 0,08 | 16 |
| Налтрексон[6] | 0,26 | 5,15 | 117 |
Биодоступность
Благодаря наличию метиленовой группы, налмефен не подвергается пресистемному метаболизму по положению 6, что отличает его от налтрексона, низкая (5 %) пероральная биодоступность которого связана с восстановлением кетоновой группы в положении 6, при первом прохождении через печень. Такое повышение метаболической стабильности увеличивает абсолютную биодоступность, которая для налмефена составляет 41 %. Одновременный прием с пищей с высоким содержанием жиров увеличивает общую экспозицию (AUC) на 30 % и Cmax на 50 %, при этом Tmax в плазме крови увеличивается на 30 мин[7].
Распределение
Связывание с белками плазмы составляет около 30 %. Кажущийся Vd — около 3200 л[7].
Биотрансформация
При приеме внутрь налмефен подвергается экстенсивному метаболизму до основного метаболита налмефен-3-О-глюкуронида, главным образом под действием изофермента UGT2B7 и в меньшей степени за счет изоферментов UGT1A3 и UGT1A8. Относительно небольшое количество налмефена метаболизируется до норналмефена под действием изофермента CYP3A4/5 и налмефен-3-О-сульфата сульфированием. Норналмефен в свою очередь превращается в норналмефен-3-О-глюкуронид и норналмефен-3-О-сульфат. Метаболиты не вносят значимого вклада в фармакодинамические эффекты, связанные с воздействием на опиоидные рецепторы у людей, за исключением налмефен-3-О-сульфата, который имеет сравнимую с налмефеном активность. Однако концентрация налмефен-3-О-сульфата составляет менее 10 % от концентрации налмефена. По этой причине маловероятно, что данный метаболит вносит значимый вклад в развитие фармакологических эффектов налмефена[7].
Выведение
Конъюгация с глюкуроновой кислотой является главным механизмом, определяющим клиренс налмефена. Почечная экскреция является основным путём выведения метаболитов налмефена. Конечный T1/2 равен 12,5 ч[7].
Фармакодинамически-фармакокинетические соотношения
По данным позитронно-эмиссионного сканирования, после перорального приема налмефена в дозе 20 мг, оккупированость (процент рецепторов, связанных с лигандом в конкретный момент времени) центральных μ-опиоидных рецепторов уже через 3 ч составляет более 90 % и сохраняется приблизительно на таком же уровне в течение последующих 26 часов[8] , что сопоставимо с аналогичными параметрами налтрексона[9]. Поскольку оккупированность рецепторов является функцией от константы аффинности (Ki), очевидно, что «насыщение» налмефеном популяции КОР рецепторов будет выше и более продолжительным, чем МОР.
Режим дозирования
Алкогольная зависимость
Начинать приём налмефена следует лишь при отсутствии физических признаков острого синдрома отмены алкоголя. «Селинкро» рекомендовано применять в сочетании с продолжительной психосоциальной поддержкой, направленной на сохранение приверженности лечению и снижение потребления алкоголя[7].
Для лечения алкогольной зависимости налмефен принимается внутрь в дозе 18 мг в сутки.
Налмефен применяется в режиме «по необходимости». Такой режим предполагает гибкий подход к приему препарата: в дни, когда существует риск приема алкоголя, пациент принимает 1 таблетку (18 мг) утром, либо за 1-2 часа до приема алкоголя. Если пациент начал употреблять алкоголь, не приняв предварительно препарат, ему следует это сделать как можно быстрее [налмефен не имеет риска нежелательных взаимодействий с алкоголем].
Режим «по необходимости» по определению может трактоваться и как ежедневный поддерживающий прием препарата. Ежедневный примем налмефена представляется наиболее рациональным в течение первых месяцев терапии, особенно у пациентов с частыми алкогольными эксцессами, а также в случае неоднократных прецедентов пропуска заблаговременного приема препарата в связи с высокой импульсивностью или анозогнозией. Не исключено, что ежедневное применение может иметь дополнительные клинические преимущества, особенно у пациентов склонных к дисфориям, ангедонии и с коморбидными аффективными нарушениями[10].
Непрерывная психосоциальная поддержка, рекомендуемая наряду с использованием Селинкро, является простым вмешательством. Главной его целью является поддержка пациента в стремлении снизить потребление алкоголя и улучшить приверженность лечению, что может быть достигнуто во время обычной консультации врача общей практики или другого медицинского работника первичного звена здравоохранения[11].
Антидот наркотических анальгетиков
Для частичного купирования послеоперационной опиоидной седации, препарат «Revex» (раствор 0,1 мг/мл) применялся внутривенно в дозе 0,025—0,1 мг (на пациента весом 100 кг). Использование в анестезиологии доз, не превышающих 1 мкг/кг, позволяет купировать избыточный седативный эффект наркотических анальгетиков, без значимого снижения анальгетического. Ввиду быстрого распределения препарата в организме, продолжительность действия парентеральных доз, не превышающих 1 мкг/кг, составляет 30—60 мин.
В качестве антидота при передозировке опиоидов препарат «Revex» (раствор 1 мг/мл) применялся внутривенно в дозе 0,5—1,5 мг (на пациента весом 70 кг). Действие абсолютной купирующей дозы (1 мг на пациента весом 70 кг) продолжается в течение многих часов. Анальгетический эффект опиоидных анальгетиков в течение данного периода времени полностью аннулируется. По этой причине, при подозрении на наличие физической зависимости от опиоидов у лиц с передозировкой, применение налмефена было рекомендовано начинать с введения дозы 0,1 мг. Введение абсолютной купирующей дозы налмефена возможно лишь в случае отсутствия симптомов отмены опиоидов в течение последующих 2 минут[2].
Клиническая эффективность
Сокращение потребления алкоголя признается Всемирной организацией здравоохранения (ВОЗ), Европейской медицинской ассоциацией (ЕМА) и руководством общественного здравоохранения в качестве приемлемой терапевтической цели для пациентов, страдающих алкогольной зависимостью[12][13][14][15][16].
Налмефен, принимаемый «по необходимости», дает пациенту возможность контролировать ситуацию, управляя болезнью и лечением[11].
Налмефен изучался в трех регистрационных клинических исследованиях III фазы: ESENSE1, ESENSE2 и SENSE, в которых участвовали 1 997 пациентов с алкогольной зависимостью. Одна группа получала налмефен и психосоциальную поддержку, другая — плацебо и психосоциальную поддержку. Исследования ESENSE1 и ESENSE2 имели две первичные конечные точки: (1) сокращение числа дней тяжелого пьянства и (2) сокращение суммарного потребления алкоголя[11].
Было показано, что через 6 месяцев приема налмефена потребление алкоголя снижается более чем на 60 %[17][18].
Анализ вторичных конечных точек показал, что налмефен улучшает качество жизни, связанное со здоровьем (по шкалам HRQoL, SF-36 и EQ-5D)[11].
В исследование SENSE также включались пациенты с коморбидными аффективными расстройствами (текущими или в анамнезе). Было показано, что к 13 месяцу терапии, в группе налмефена наблюдалось более выраженное улучшение настроения по шкале аффективного профиля (POMS), чем в группе плацебо. Тем не менее, ввиду небольшой пропорции таких пациентов (35 человек) в данном исследовании, выводы об эффективности налмефена в отношении коморбидных аффективных нарушений следует делать с осторожностью[10]. Тем не менее, эти данные лишь подтверждают теоретические предположения о возможном наличии у налмефена антидепрессивного, анксиолитического и антиангедонического действия, логически проистекающие из его функционального антагонизма к КОР рецептору, в условиях, связанных с чрезмерным повышением уровня эндогенного динорфина.
Безопасность
Наиболее распространенными нежелательными явлениями, возникавшими чаще на фоне налмефена, чем плацебо, были тошнота, головокружение, бессонница, головная боль, рвота, слабость и сонливость.
Большинство нежелательных явлений имели легкую или среднюю степень тяжести, и наблюдались главным образом в начале лечения.
Частота отказов от лечения из-за побочных эффектов была схожей в группе налмефена и плацебо[11].
См. также
Примечания
- US patent 3814768, Jack Fishman et al, «6-METHYLENE-6-DESOXY DIHYDRO MORPHINE AND CODEINE DERIVATIVES AND PHARMACEUTICALLY ACCEPTABLE SALTS», published 1971-11-26, issued 1974-06-04
- http://www.accessdata.fda.gov/drugsatfda_docs/label/2006/020459s006lbl.pdf
- Drugs@FDA: FDA Approved Drug Products. www.accessdata.fda.gov. Дата обращения: 20 марта 2016.
- Philippe Laramée, Thor-Henrik Brodtkorb, Nora Rahhali, Chris Knight, Carolina Barbosa. The cost-effectiveness and public health benefit of nalmefene added to psychosocial support for the reduction of alcohol consumption in alcohol-dependent patients with high/very high drinking risk levels: a Markov model // BMJ open. — 2014-01-01. — Т. 4, вып. 9. — С. e005376. — ISSN 2044-6055. — doi:10.1136/bmjopen-2014-005376.
- Bart G., Schluger J.H., Borg L., Ho A., Bidlack J.M., Kreek M.J. Nalmefene induced elevation in serum prolactin in normal human volunteers: partial kappa opioid agonist activity? (англ.) // Neuropsychopharmacology : journal. — 2005. — Vol. 30, no. 12. — P. 2254—2262. — doi:10.1038/sj.npp.1300811. — PMID 15988468.
- Li G, Aschenbach LC, Chen J, et al. Design, Synthesis, and Biological Evaluation of 6α- and 6β-N-Heterocyclic Substituted Naltrexamine Derivatives as μ Opioid Receptor Selective Antagonists. Journal of medicinal chemistry. 2009;52(5):1416-1427. doi:10.1021/jm801272c.
- Инструкция по медицинскому применению препарата Селинкро. Регистр лекарственных средств РФ..
- Ingman K, Hagelberg N, Aalto S, Någren K, Juhakoski A, Karhuvaara S, Kallio A, Oikonen V, Hietala J, Scheinin H. Prolonged central mu-opioid receptor occupancy after single and repeated nalmefene dosing. Neuropsychopharmacology. 2005 Dec;30(12):2245-53.
- Lee MC, Wagner HN Jr, Tanada S, Frost JJ, Bice AN, Dannals RF. Duration of occupancy of opiate receptors by naltrexone. J Nucl Med. 1988 Jul;29(7):1207-11.
- P.6.b.016 Effect of nalmefene as needed on alcohol consumption and mood in alcohol dependent patients with comorbid mood disorder - European Neuropsychopharmacology. www.europeanneuropsychopharmacology.com. Дата обращения: 31 марта 2016.
- Обзор данных по препарату Селинкро® (налмефен), расширяющему возможности терапии алкогольной зависимости (резюме рандомизированных контролируемых исследований). Обозрение психиатрии и медицинской психологии имени В. М. Бехтерева | № 4, 2014
- National Institute on Alcohol Abuse and Alcoholism (NIAAA). Helping patients who drink too much. A clinician’s guide. Updated 2005 Edition. National Institutes of Health (NIH) Publication No. 07-3769. 2007.
- National Institute on Alcohol Abuse and Alcoholism (NIAAA). Rethinking drinking: alcohol and your health. National Institutes of Health (NIH) Publication No. 10-3770. 2010.
- National Institute of Health and Clinical Excellence. Alcohol-use disorders: preventing harmful drinking. NICE public health guidance 24. Issued: June 2010. © NICE 2010. guidance.nice.org.uk/ph24
- European Medicines Agency (EMA). Committee for Medicinal Products for Human use (CHMP). Guideline on the development of medicinal products for the treatment of alcohol dependence. EMA/CHMP/EWP/20097/2008. 2010
- WHO (2001) «Th world health report 2001 — mental health: new understanding, new hope.» http://www.who.int/whr/2001/en/
- Wim van den Brink, Henri-Jean Aubin, Anna Bladström, Lars Torup, Antoni Gual. Efficacy of as-needed nalmefene in alcohol-dependent patients with at least a high drinking risk level: results from a subgroup analysis of two randomized controlled 6-month studies // Alcohol and Alcoholism (Oxford, Oxfordshire). — 2013-10-01. — Т. 48, вып. 5. — С. 570—578. — ISSN 1464-3502. — doi:10.1093/alcalc/agt061.
- Wim van den Brink, Per Sørensen, Lars Torup, Karl Mann, Antoni Gual. Long-term efficacy, tolerability and safety of nalmefene as-needed in patients with alcohol dependence: A 1-year, randomised controlled study // Journal of Psychopharmacology (Oxford, England). — 2014-08-01. — Т. 28, вып. 8. — С. 733—744. — ISSN 1461-7285. — doi:10.1177/0269881114527362.