Эверолимус
Эверолимус — является производным сиролимуса (рапамицина) и имеет такой же механизм действия как и сиролимус, обладает иммуносупрессивным и противоопухолевым действием, является ингибитором mTOR.[2]
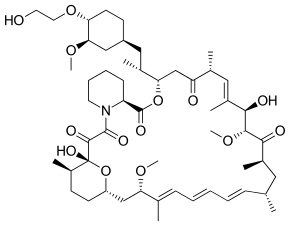
| Эверолимус | |
|---|---|
 | |
 | |
| Химическое соединение | |
| ИЮПАК | dihydroxy-12-[(2R)-1-[(1S,3R,4R)-4-(2-hydroxyethoxy)-3-methoxycyclohexyl]propan-2-yl]-19,30-dimethoxy-15,17,21,23,29,35-hexamethyl-11,36-dioxa-4-azatricyclo[30.3.1.0 hexatriaconta-16,24,26,28-tetraene-2,3,10,14,20-pentone |
| Брутто-формула | C53H83NO14 |
| Молярная масса | 958.224 г/моль |
| CAS | 159351-69-6 |
| PubChem | 6442177 |
| DrugBank | DB01590 |
| Состав | |
| Классификация | |
| АТХ | L01XE10, L04AA18 |
| Фармакокинетика | |
| Период полувывед. | ~30 hours[1] |
| Способы введения | |
| Oral | |
Фармакологическое действие
Иммунодепрессивное средство, ингибитор пролиферативного сигнала. Оказывает иммуносупрессивный эффект путём ингибирования антиген-активированной пролиферации Т-клеток, клональной экспансии, вызываемой интерлейкинами Т-клеток (интерлейкин-2, интерлейкин-15). Ингибирует внутриклеточный сигнальный путь, который в норме приводит к клеточной пролиферации, запускаемой связыванием факторов роста Т-клеток с соответствующими рецепторами. Блокада сигнала приводит к остановке деления клеток на стадии G1 клеточного цикла. На молекулярном уровне образует комплекс с цитоплазматическим белком FKBP-12. Происходит ингибирование фосфорилирования р70 S6 киназы, стимулируемой фактором роста. Фосфорилирование р70 S6 киназы находится под контролем FRAP, то есть комплекс эверолимус-FКВР-12 связывается с FRAP. FRAP — это ключевой регуляторный белок, который управляет клеточным метаболизмом, ростом и пролиферацией; нарушение его функций объясняет остановку клеточного цикла, вызываемую эверолимусом. Эверолимус имеет отличный от циклоспорина механизм действия. Комбинация эверолимуса с циклоспорином более эффективна, чем при изолированном использовании каждого из них. Эверолимус ингибирует пролиферацию гемопоэтических и негемопоэтических клеток (гладкомышечных клеток). Пролиферация гладкомышечных клеток сосудов, запускаемая при повреждении эндотелиальных клеток, приводит к образованию неоинтимы, которая играет ключевую роль в патогенезе хронического отторжения.
Фармакокинетика
Биодоступность диспергируемых таблеток (по сравнению с обычной таблеткой) составляет 0,9. TCmax — 1-2 ч. TCss — на 4-й день. При применении в дозах 0,75 мг и 1,5 мг 2 раза в сутки Cmax — 6,5-15,7 и 12,3-28,3 нг/мл соответственно; AUC — 44-106 и 72-160 нг•х ч/мл соответственно. При применении в дозах 0,5 мг и 1,5 мг 2 раза в сутки базальная концентрация в крови (определяется утром до приема очередной дозы) составляет 2,0-6,2 и 2,5-11,7 нг/мл соответственно. Базальная концентрация коррелирована с AUC (коэффициент корреляции 0,86-0,94). Концентрация в крови пропорциональна принятой дозе (в диапазоне доз 0,5-15 мг). Соотношение концентрации в крови и концентрации в плазме составляет 17-73 % (зависит от значений концентрации в диапазоне — 5-5000 нг/мл). При приеме таблеток с очень жирной пищей Cmax и AUC уменьшаются на 60 % и 16 % соответственно. Связь с белками — 74 %. Объём распределения — 235—449 л; объём распределения (в равновесном состоянии) — 110 л (отклонение 36 %). Эверолимус является субстратом CYP3A4 и Р-гликопротеина. Основные пути метаболизма — моногидроксилирование и О-дезалкилирование. Два основных метаболита образуются путём гидролиза циклического лактона и не имеют существенной иммуносупрессивной активности. Общий клиренс — 8, л/ч (отклонение — 27 %). T1/2 — 21-35 ч. Выводится кишечником (80 %) и почками (5 %). У пациентов с печеночной недостаточностью (класс В по шкале Чайлд-Пьюга) AUC увеличивается в 2 раза. Показатель AUC положительно коррелирует с концентрацией билирубина и увеличением протромбинового времени и отрицательно — с концентрацией сывороточного альбумина. У детей от 1 года до 16 лет клиренс линейно повышается в зависимости от возраста, площади поверхности тела (0,49-1,92 м²), массы тела (11-77 кг); в равновесном состоянии клиренс составляет 7,2-12,2 л/ч/м²; T1/2 — 19-41 ч. У детей 1-16 лет, получающих эверолимус в форме диспергируемых таблеток в дозе 0,8 мг/м (максимально 1,5 мг) 2 раза в сутки с циклоспорином (микроэмульсия), AUC — 60-114 нг•х ч/мл, что соответствует таковой у взрослых, получающих препарат в дозе 0,75 мг 2 раза в сутки. Базальная концентрация в равновесном состоянии — 2,7-6,1 нг/мл. У пациентов в возрасте 16-70 лет наблюдалось снижение клиренса на 0,3 % в год. Общий клиренс у пациентов негроидной расы выше на 20 %. Базальная концентрация эверолимуса, частота острого отторжения и тромбоцитопении связаны между собой (у реципиентов трансплантата почки и сердца в течение 6 мес после трансплантации). Экспозиция эверолимуса остается стабильной все время в течение первого года после трансплантации. Фармакокинетика у пациентов с почечным и сердечным трансплантатом, получающих эверолимус 2 раза в сутки одновременно с циклоспорином (в форме микроэмульсии), сопоставима.
Показания
Профилактика отторжения трансплантата у взрослых реципиентов трансплантата почки и сердца с низким и средним иммунологическим риском, получающих базовую иммуносупрессивную терапию циклоспорином (в виде микроэмульсии) и ГКС.
Распространенный и/или метастатический почечно-клеточный рак (при неэффективности антиангиогенной терапии). Рак молочной железы, рак почек, нейроэндокринные опухоли поджелудочного происхождения, клубневый склероз.
Противопоказания
Гиперчувствительность, детский возраст.
С осторожностью
Печеночная недостаточность, ХПН, беременность. Для ЛФ, содержащих лактозу (дополнительно): наследственная непереносимость галактозы, лактазная недостаточность, глюкозо-галактозная мальабсорбция.
Дозирование
Внутрь, только с пищей или без неё (для минимальной вариабельности), сразу после трансплантации, одновременно с циклоспорином (микроэмульсия); таблетки проглатывают целиком, запивая стаканом воды (или в виде диспергируемых таблеток) по 0,5 мг 2 раза в сутки. Через 4-5 дней проводят коррекцию режима дозирования (на основе базальной концентрации эверолимуса).
При печеночной недостаточности (класс А или В по шкале Чайлд-Пьюга) дозу уменьшают в 2 раза (по сравнению со средней дозой) в случаях, когда имеется сочетание двух из показателей: билирубин более 34 мкмоль/л, альбумин менее 35 г/л, протромбиновое время более 1,3 по МНО (увеличение более 4 с). Дозу титруют, основываясь на терапевтический мониторинг.
Представителям негроидной расы (по ограниченной информации) может потребоваться более высокая доза для достижения такого же эффекта, как у остальных пациентов, получающих препарат в рекомендуемых для взрослых дозах.
Побочное действие
Частота: очень часто (более 1/10), часто (более 1/100 и менее 1/10), нечасто (более 1/1000 и менее 1/100), редко (более 1/10 000 и менее 1/1000), очень редко (менее 1/10000).
Со стороны органов кроветворения: очень часто — лейкопения (дозозависима, чаще при дозе 3 мг/сут); часто — тромбоцитопения (дозозависима, чаще при дозе 3 мг/сут), анемия (дозозависима, чаще при дозе 3 мг/сут), коагулопатия, тромботическая тромбоцитопеническая пурпура/гемолитико-уремический синдром; нечасто — гемолиз.
Со стороны обмена веществ: очень часто — гиперхолестеринемия, гиперлипидемия; часто — гипертриглицеридемия.
Со стороны ССС: часто — повышение АД, лимфоцеле (при трансплантации почки), флеботромбоз.
Со стороны дыхательной системы: часто — пневмония; нечасто — пневмонит.
Со стороны пищеварительной системы: часто — абдоминальная боль, диарея, тошнота, рвота.
Со стороны кожных покровов: часто — ангионевротический отек (при одновременном приеме ингибиторов АПФ), угри, осложнения со стороны хирургической раны; нечасто — сыпь.
Со стороны опорно-двигательного аппарата: нечасто — миалгия.
Со стороны мочеполовой системы: часто — инфекции мочевыводящих путей; нечасто — некроз почечных канальцев, пиелонефрит, гипогонадизм у мужчин (снижение концентрации тестостерона, повышение концентрации ЛГ).
Прочие: часто — вирусные, бактериальные, грибковые инфекции, сепсис, отеки, боль; нечасто — раневая инфекция, гепатит, нарушения функции печени, желтуха, повышение АЛТ, ACT, ГГТ.
Возможно (у пациентов, наблюдавшихся не менее 1 года) возникновение лимфом или лимфопролиферативных заболеваний (у 1,4 % пациентов, получавших эверолимус по 1,5 мг или 3 мг/сут, в комбинации с др. иммунодепрессантами); злокачественных новообразований кожи (у 1,3 % пациентов), др. типов малигнизации (у 1,2 % пациентов).
Передозировка
Лечение: симптоматическое.
Взаимодействие
Метаболизируется при участии изофермента CYP3A4, является субстратом для белка-переносчика Р-гликопротеина, следовательно, применение с мощными ингибиторами или индукторами CYP3A4 не рекомендуется.
Ингибиторы Р-гликопротеина могут снизить высвобождение эверолимуса из кишечных клеток и повысить его концентрацию в сыворотке.
Эверолимус являлся конкурентным ингибитором CYP3A4 и CYP2D6, потенциально увеличивающим концентрации ЛС, метаболизирующихся при участии этих ферментов. Следует соблюдать осторожность при одновременном применении эверолимуса с субстратами CYP3A4 и CYP2D6, имеющими узкий терапевтический индекс.
Биодоступность эверолимуса значительно увеличивается при одновременном применении циклоспорина (ингибитор CYP3A4/Р-гликопротеина).
Циклоспорин в виде микроэмульсии увеличивает AUC эверолимуса на 168 % (46-365 %) и Cmax — на 82 % (25-158 %) по сравнению с применением только одного эверолимуса. При изменении дозы циклоспорина может потребоваться коррекция дозы эверолимуса.
Клиническая значимость влияния эверолимуса на фармакокинетику циклоспорина минимальна у пациентов с пересадкой почки и сердца, получающих циклоспорин в форме микроэмульсии.
Применение эверолимуса после многократных доз рифампицина (индуктор CYP3A4), повышает клиренс эверолимуса в 3 раза, уменьшает Cmax на 58 % и AUC — на 63 %.
Комбинированное применение эверолимуса с рифампицином не рекомендуется.
Прием однократной дозы эверолимуса с аторвастатином (субстрат CYP3A4) или правастатином (субстрат Р-гликопротеина) не оказывает клинического влияния на фармакокинетику аторвастатина, правастатина, эверолимуса и на общую биореактивность ГМГ-КоА-редуктазы в плазме. Однако эти результаты не учитывают действие др. ингибиторов ГМГ-КоА-редуктазы. Пациентов, получающих ингибиторы ГМГ-КоА-редуктазы, следует наблюдать на предмет развития рабдомиолиза и др. нежелательных явлений.
Умеренные ингибиторы CYP3A4 и Р-гликопротеина (флуконазол, эритромицин, верапамил, никардипин, дилтиазем, нелфинавир, индинавир, ампренавир) могут повышать концентрацию эверолимуса в крови.
Индукторы CYP3A4 (зверобой продырявленный, карбамазепин, фенобарбитал, фенитоин, эфавиренз, невирапин) могут повышать метаболизм эверолимуса и снижать его концентрацию в крови.
Грейпфрутовый сок влияет на активность цитохрома Р450 и Р-гликопротеина, поэтому следует избегать его одновременного применения с эверолимусом.
На фоне лечения эверолимусом вакцинация может быть менее эффективной. Следует избегать использования живых вакцин.
Особые указания. Лечение должны проводить только врачи, имеющие опыт иммуносупрессивной терапии после трансплантации органов, и возможность мониторинга концентрации эверолимуса в цельной крови.
У пациентов с базальной концентрацией 3 нг/мл и более частота острого отторжения (почки и сердца) ниже, чем у пациентов с базальной концентрацией менее 3 нг/мл.
Рекомендуемый верхний предел терапевтической концентрации эверолимуса — 8 нг/мл.
У пациентов с печеночной недостаточностью при одновременном применении мощных индукторов и ингибиторов CYP3A4, при переходе на др. ЛФ и/или если доза циклоспорина значительно снижена, необходимо контролировать концентрацию эверолимуса в крови.
Концентрации эверолимуса при применении диспергируемых таблеток несколько ниже, чем при применении обычных таблеток.
Поскольку циклоспорин взаимодействует с эверолимусом, возможно снижение концентрации последнего, если концентрация циклоспорина существенно снижается (базальная концентрация менее 50 нг/мл).
Эверолимус не следует применять длительно с циклоспорином в полной дозе. Снижение дозы циклоспорина начинают через 1 мес после почечной трансплантации, что приводит к улучшению функции почек.
Рекомендуемая концентрация циклоспорина (через 2 ч после приема): 0-4 нед — 1000—1400 нг/мл; 5-8 нед — 700—900 нг/мл; 9-12 нед — 550—650 нг/мл; 13-52 нед — 350—450 нг/мл. При этом базальная концентрация циклоспорина должна составлять (нг/мл): 1-й мес — 125—353; 3-й мес — 46-216; 6-й мес — 22-142; 12-й мес — 33-89.
Очень важно (в раннем периоде после трансплантации), чтобы концентрации эверолимуса и циклоспорина не снижались ниже терапевтического диапазона, с целью минимизации риска отсутствия эффекта. До снижения дозы циклоспорина следует уточнить, что равновесная концентрация эверолимуса 3 нг/мл и более.
Существуют ограниченные данные по применению эверолимуса при базальной концентрации циклоспорина менее 50 нг/мл или концентрации циклоспорина в поддерживающей фазе менее 350 нг/мл.
Если пациент не переносит снижение дозы циклоспорина, то следует пересмотреть последующее использование эверолимуса.
У пациентов после трансплантации сердца в поддерживающей фазе следует снижать дозу циклоспорина для улучшения функции почек.
При ухудшении функции почек или если КК менее 60 мл/мин, необходима коррекция режима терапии. Дозу циклоспорина устанавливают на основании его базальной концентрации.
При пересадке сердца имеются ограниченные данные по применению эверолимуса при базальной концентрации циклоспорина менее 175 нг/мл в первые 3 мес; менее 135 нг/мл — на 6-й мес; менее 100 нг/мл — после 6 мес.
Эверолимус применяют одновременно с циклоспорином в форме микроэмульсии, базиликсимабом и ГКС.
Не рекомендуется совместное применение с мощными ингибиторами CYP3A4 (кетоконазол, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир) и индукторами (рифампицин, рифабутин), за исключением тех случаев, когда ожидаемая польза терапии превышает потенциальный риск.
Необходимо контролировать концентрации эверолимуса в крови при одновременном применении с индукторами или ингибиторами CYP3A4 и после их отмены.
В период лечения следует контролировать состояние пациентов для выявления кожных новообразований; необходимо свести к минимуму воздействие УФ-излучения, солнечного света, использовать соответствующие солнцезащитные средства. Риск возникновения кожных новообразований связан скорее с длительностью и интенсивностью иммуносупрессии, чем с использованием конкретного препарата. Чрезмерная иммуносупрессия предрасполагает к развитию инфекций, особенно оппортунистических. Имеются сообщения о развитии фатальных инфекций и сепсиса.
В течение 3 мес после трансплантации рекомендуют проводить профилактику ЦМВ-инфекции (у пациентов с повышенным риском развития инфекции).
Совместное применение эверолимуса с циклоспорином (микроэмульсия) повышает содержание в сыворотке холестерина и ТГ, что может потребовать соответствующего лечения. Пациентов следует наблюдать с целью выявления гиперлипидемии, при необходимости проводить лечение гиполипидемическими ЛС и назначать соответствующую диету.
В случае выявления гиперлипидемии при назначении иммуносупрессивных ЛС, необходимо оценить соотношение риск/польза.
Следует оценивать соотношение риск/польза продолжения терапии эверолимусом у пациентов с тяжелой рефрактерной гиперлипидемией. Пациентов, получающих ингибиторы ГМГ-КоА-редуктазы и/или фибраты, следует наблюдать на предмет развития нежелательных явлений, вызванных вышеуказанными ЛС.
Во время лечения всем пациентам рекомендуется контроль функции почек. При повышении КК следует решить вопрос о коррекции иммуносупрессивной терапии (уменьшение дозы циклоспорина).
Следует соблюдать осторожность при одновременном применении др. ЛС, оказывающих отрицательное влияние на функцию почек. Имеются ограниченные данные по применению эверолимуса у детей при трансплантации почек.
У пациентов с печеночной недостаточностью следует тщательно мониторировать базальную концентрацию эверолимуса в цельной крови.
Женщинам детородного возраста следует рекомендовать использовать эффективные методы контрацепции в период лечения и в течение 8 нед после окончания терапии.
Ссылки
- R.N Formica Jra, K.M Lorberb, A.L Friedmanb, M.J Biaa, F Lakkisa, J.D Smitha, M.I Lorber. The evolving experience using everolimus in clinical transplantation (англ.) // Elsevier : journal. — 2004. — March (vol. 36, no. 2). — P. S495—S499. — doi:10.1016/j.transproceed.2004.01.015.
- Novartis (2009-03-30). Afinitor approved in US as first treatment for patients with advanced kidney cancer after failure of either sunitinib or sorafenib. Пресс-релиз. Архивировано из первоисточника 3 апреля 2009. Проверено April 6, 2009.