Аллофикоцианин
Аллофикоцианин (от Греческого: ἄλλος (аллос) — «другой», φύκος (фикос) — «водоросль», и κυανός (кианос) — «голубой») — светособирающий белок из семейства фикобилипротеинов, в которое так же входят фикоцианин, фикоэритрин и фикоэритроцианин, и является вспомогательным пигментом для хлорофилла. Все фикобилипротеины растворимы в воде и следовательно не могут быть закреплены на мембране как каротиноиды, а вместо этого формируют закреплённые на мембране кластеры, называемые фикобилисомами. Аллофикоцианин поглощает и излучает красный свет (650 и 660 нм соответственно), и легко обнаруживается у цианобактерий и красных водорослях. Способность фикобилинов испускать свет используется в наборах иммунологического анализа. Аллофикоцианин довольно часто используют в проточной цитометрии, при счёте и сортировке клеток, и микроскопии. Для этого в него внедряют химическую сшивку.
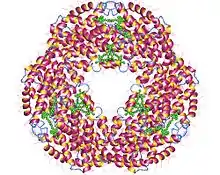
Строение
Аллофикоцианин можно выделить из разных видов красных или сине-зелёных водорослей, каждый из которых синтезирует свою, несколько отличающуюся от других форму этой молекулы. Белок состоит из двух типов субъединиц (α и β), каждая несёт по одной хромофорной группе фикоцианобилина. Общую формулу белка можно описать как (αβ)3. Молекулярная масса аллофикоцианина 105 кДа.
Спектральные характеристики
| Максимум поглощения | 652 нм |
| Добавочный максимум поглощения | 625 нм |
| Максимум излучения | 657.5 нм |
| Сдвиг Стокса | 5.5 нм |
| Коэффициент экстинкции | 2.4 x 105 M−1см−1 |
| Квантовый выход | 0.68 |
| Яркость | 1.6 x 105 M−1см−1 |
Сшитый аллофикоцианин
Как упоминалось выше, чтобы использовать аллофикоцианин в иммунологическом анализе, его необходимо химически сшить, чтобы предотратить диссоциацию его субъединиц, что довольно часто происходит в стандартных физиологических буферах.[1] Традиционным методом для этого служит смешивание с 1-этил-3,3-диметиламинопропилом — мощным сшивочным агентом. Затем его обрабатывают восьми молярным раствором мочевины, а затем дают ренатурировать, но уже в физиологическом буфере. Такая процедура позволяет избавится от несшившихся субъединиц.[2] Существуют альтернативные способы, использование которых позволяет сохранить нативную структуру тримера и получить более яркий конечный продукт[3].
Примечания
- George C. Papageorgiou, Thoula Lagoyanni. Effects of chaotropic electrolytes on the structure and electronic excitation coupling of glutaraldehyde- and diimido ester-cross-linked phycobilisomes. Biochimica et Biophysica Acta (BBA) — Bioenergetics Volume 724, Issue 3, 30 September 1983, Pages 323—332
- Yeh SW, Ong LJ, Clark JH, Glazer AN. Fluorescence properties of allophycocyanin and a crosslinked allophycocyanin trimer. Cytometry. 1987 Jan; 8(1):91-5.
- United States Patent 7256050; High fluorescent intensity cross-linked allophycocyanin. Assigned to Columbia Biosciences Corp.